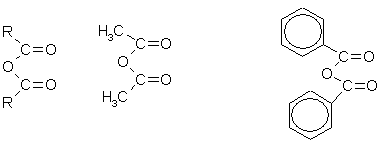ნიტრილები დასახელებულია სხვადასხვა გზით:
CH 3 CN CH 2 \u003d CHCN PhCN NC (CH 2) 4 CN
ეთანენიტრილი პროპენნიტრილი ბენზოლეკარბონიტრილი ადიპონიტრილი
(აცეტონიტრილი) (აკრილონიტრილი) (ბენზონიტრილი)
ნიტრილების მიღების მეთოდები
3.1.1. ნიტრილების მიღება ამიდების დეჰიდრატაციით
ამიდების დეჰიდრატაცია, რომელიც წინა ნაწილში განვიხილეთ, შეიძლება გახდეს კარბოქსილის მჟავის ამ მჟავის ნიტრილად გარდაქმნის ჯაჭვის ბოლო ნაბიჯი:
ყველა ეს რეაქცია ხშირად გაერთიანებულია ერთ პროცესში, კარბოქსილის მჟავისა და ამიაკის ნარევი ალუმინის გავლით 500 o C ტემპერატურაზე:
სავარჯიშო 46.დაწერეთ ადიპინის მჟავიდან ადიპონიტრილის მიღების სამრეწველო მეთოდის რეაქცია.
3.1.2. ნიტრილების მიღება ნახშირწყალბადების ოქსიდაციური ამმონოლიზით
ნახშირწყალბადების დაჟანგვის შესწავლისას ვნახეთ, რომ ჰიდროციანმჟავა (ჭიანჭველა მჟავა ნიტრილი) და სხვა მჟავების ნიტრილები მიიღება შესაბამისი ნახშირწყალბადების ჟანგვითი ამონოლიზით სქემის მიხედვით:
სავარჯიშო 47.დაწერეთ რეაქციები ა) აკრილონიტრილის, ბ) ბენზონიტრილის, გ) აცეტონიტრილის და დ) ტერეფტალის მჟავას ნიტრილის მისაღებად შესაბამისი ნახშირწყალბადების ოქსიდაციური მონოლიზით.
3.1.3. ნიტრილების მიღება კოლბის რეაქციით
როდესაც ჰალოკარბონები ურთიერთქმედებენ კალიუმის ციანიდთან წყალხსნარში ეთანოლში, ნიტრილები წარმოიქმნება S N 2 მექანიზმით:
ვინაიდან ციანიდის ანიონი არის ამბიდენტური იონი, იზონიტრილები წარმოიქმნება როგორც ქვეპროდუქტი, რომლებიც ამოღებულია სარეაქციო ნარევის განზავებული მარილმჟავით შერყევის შედეგად.
სავარჯიშო 48.დაწერეთ რეაქციები ეთილენიდან პროპიონიტრილის, ბ) პროპილენიდან ბუტირონიტრილის, გ) ეთილენისგან სუქცინის დინიტრილის მისაღებად, პროპილენიდან ვინილძმარმჟავას ნიტრილის, ე) ტოლუოლისგან ფენილძმარმჟავას ნიტრილის, ე) ფენილ ძმარმჟავას ნიტრილის მისაღებად. მჟავა ნიტრილი ტოლუოლიდან, (ვ) ადიპინის მჟავა დინიტრილი აცეტილენიდან.
სავარჯიშო 49.სრული რეაქციები:
ნიტრილების რეაქციები
3.2.1. ნიტრილების ჰიდროგენიზაცია
ნიტრილები ადვილად ჰიდროგენდება ამინებში. ჰიდროგენიზაცია ხორციელდება ან წყალბადით იზოლაციის დროს (C 2 H 5 OH + Na) ან კატალიზურად:
სავარჯიშო 50.დაწერეთ (ა) პროპიონიტრილის, (ბ) ბუტირონიტრილის, (გ) სუქცინის მჟავას დინიტრილის, (დ) ვინილძმარმჟავას ნიტრილის, (ე) ფენილძმარმჟავას ნიტრილის, (ვ) ადიპინის მჟავას დინიტრილის ჰიდროგენაციის რეაქციები.
3.2.2. ნიტრილების ჰიდროლიზი
ნუკლეოფილური ჩანაცვლების რეაქციით ალკილის ჰალოიდებიდან და მეტალის ციანიდებიდან მიღებული ნიტრილები კარგი საწყისი პროდუქტია კარბოქსილის მჟავების მოსამზადებლად. ამისათვის ისინი ექვემდებარებიან ჰიდროლიზს მჟავების ან ფუძეების თანდასწრებით:

სავარჯიშო 51.რა მჟავები წარმოიქმნება შემდეგი ნიტრილების ჰიდროლიზის დროს:
(ა) პროპიონიტრილი, (ბ) ბუტირონიტრილი, (გ) სუქცინის მჟავა დინიტრილი, (დ) ვინილძმარმჟავას ნიტრილი, (ე) ფენილძმარმჟავას ნიტრილი, (ვ) ადიპინის მჟავა დინიტრილი.
ამ სქემის მიხედვით, ფენილძმარმჟავა მიიღება ხელმისაწვდომი ბენზილის ქლორიდიდან:

სავარჯიშო 52.შემოგვთავაზეთ ტოლუენიდან დაწყებული ფენილძმარმჟავას წარმოების სქემა. აღწერეთ შესაბამისი რეაქციების მექანიზმები.
მალონის მჟავა ძირითადად მიიღება ქლოროძმარმჟავისგან სქემის მიხედვით:
სავარჯიშო 53.ეთილენისა და სხვა საჭირო რეაგენტებიდან გამომდინარე, შემოგვთავაზეთ ბუტანედიოური (საქცინის) მჟავის მიღების სქემა.
სავარჯიშო 54.შესაბამისი ჰალოკარბონების და ნიტრილების გამოყენებით, შემოგვთავაზეთ შემდეგი მჟავების მიღების სქემები: (ა) პროპიონის მჟავა ეთილენიდან, (ბ) ბუტირის მჟავა პროპილენიდან, (გ) სუქცინის მჟავა ეთილენიდან, (დ) ვინილძმარმჟავა პროპილენიდან, (ე) ტოლუოლისგან ფენილძმარმჟავა, (ე) აცეტილენისგან ადიპინის მჟავა.
ხელმისაწვდომი ციანოჰიდრინებიდან მიიღება α-ჰიდროქსი მჟავები:

სავარჯიშო 55.შესაბამის ალდეჰიდებსა და კეტონებზე და სხვა საჭირო რეაგენტებზე დაყრდნობით, შემოგვთავაზეთ სქემები (ა) 2-ჰიდროქსიოქსიპროპიონის მჟავისა და
ბ) 2-მეთილ-2-ჰიდროქსიპროპიონის მჟავა.
ნიტრილების ალკოჰოლიზი
ნიტრილები რეაგირებენ წყალბადის ქლორიდთან იმინო ქლორიდების წარმოქმნით:

მინოქლორიდი
წყალბადის ქლორიდის მოქმედება ალკოჰოლში ნიტრილებზე იწვევს იმინოესტერის ჰიდროქლორიდების წარმოქმნას, რომელთა შემდგომი ჰიდროლიზი იძლევა ეთერებს:
მეთილის მეთაკრილატი ინდუსტრიულად მიიღება აცეტონისგან ციანოჰიდრინის მეშვეობით:
აცეტონი აცეტონი ციანოჰიდრინი მეთილის მეთაკრილატი
მეთილის მეთაკრილატის პოლიმერი - პოლიმეთილ მეთაკრილატი გამოიყენება უსაფრთხოების სათვალეების (პლექსიგლასის) წარმოებაში.
მაგ. 56.რა პროდუქტი წარმოიქმნება კალიუმის ციანიდის, ეთანოლის თანმიმდევრული მოქმედების შედეგად წყალბადის ქლორიდის და ბოლოს წყალთან ბენზილქლორიდზე? დაწერეთ შესაბამისი რეაქციები.
მაგ. 57.რა პროდუქტი წარმოიქმნება აცეტალდეჰიდზე თანმიმდევრული მოქმედების შედეგად ჰიდროციანმჟავადა მერე მეთანოლი გოგირდმჟავას თანდასწრებით? დაწერეთ შესაბამისი რეაქციები.
როგორ მივიღოთ. ერთი . ალდეჰიდების და პირველადი სპირტების დაჟანგვა ჩვეულებრივი გზაა კარბოქსილის მჟავების მოსამზადებლად. გამოყენებული ჟანგვითი აგენტებია />K M n O 4 და K 2 C r 2 O 7 .
2 კიდევ ერთი გავრცელებული მეთოდია ჰალოგენირებული ნახშირწყალბადების ჰიდროლიზი, რომელიც შეიცავს სამ ჰალოგენის ატომს ერთ ნახშირბადის ატომზე. ამ შემთხვევაში წარმოიქმნება სპირტები, რომლებიც შეიცავს OH ჯგუფებს ნახშირბადის ატომში - ასეთი სპირტები არასტაბილურია და წყალს იშლება კარბოქსილის მჟავის წარმოქმნით: />
| ZNaOH | ||||
| R-CCl 3 | → | R - COOH + H 2 O | ||
| -3 NaCl |
3 . ციანიდებისგან (ნიტრილები) კარბოქსილის მჟავების მიღება მნიშვნელოვანი მეთოდია, რომელიც საშუალებას გაძლევთ შექმნათ ნახშირბადის ჯაჭვი ორიგინალური ციანიდის მიღებისას. ნახშირბადის დამატებითი ატომი შეჰყავთ მოლეკულაში ჰალოკარბონის მოლეკულაში ჰალოგენის ნატრიუმის ციანიდით ჩანაცვლების რეაქციის გამოყენებით, მაგალითად: />
CH 3 -B r + NaCN→ CH 3 - CN + NaBr.
ძმარმჟავას მიღებული ნიტრილი (მეთილციანიდი) გაცხელებისას ადვილად ჰიდროლიზდება ამონიუმის აცეტატის წარმოქმნით:
CH 3 CN + 2H 2 O → CH 3 COONH 4.
როდესაც ხსნარი მჟავდება, მჟავა გამოიყოფა:
CH 3 COONH 4 + HCl→ CH 3 COOH + NH 4 კლ.
4 . გამოყენება გრიგნარდის რეაგენტისქემის მიხედვით: />
H 2 O
R- MgBr+ CO 2 → R - COO - MgBr→ R - COOH + Mg (OH) Br
5 . ეთერების ჰიდროლიზი:/>
R - COOR 1 + KOH → R - COOK + R'OH,
R-COOK+ HCl → რ— COOH+ KCl .
6. მჟავა ანჰიდრიდების ჰიდროლიზი:/>
(RCO) 2 O + H 2 O → 2 RCOOH.
7. ცალკეული მჟავებისთვის არსებობს მომზადების სპეციფიკური მეთოდები./>
ჭიანჭველა მჟავა წარმოიქმნება ნახშირბადის მონოქსიდის გაცხელებით ( II ) დაფხვნილი ნატრიუმის ჰიდროქსიდით ზეწოლის ქვეშ და მიღებული ნატრიუმის ფორმატის დამუშავება ძლიერი მჟავით:
ძმარმჟავა მიიღება ბუტანის კატალიზური დაჟანგვით ატმოსფერული ჟანგბადით:
2C 4 H 10 + 5 O 2 → 4CH 3 COOH + 2H 2 O.
ბენზოის მჟავის მისაღებად შეიძლება გამოყენებულ იქნას მონოჩანაცვლებული ბენზოლის ჰომოლოგების დაჟანგვა კალიუმის პერმანგანატის მჟავე ხსნარით:
5C 6 H 5 -CH 3 + 6 KMnO 4 + 9 H 2 SO 4 \u003d 5C 6 H 5 COOH + 3 K 2 SO 4 + 6 MnSO 4+14H2O.
გარდა ამისა, ბენზოის მჟავის მიღება შესაძლებელია ბენზალდეჰიდის გამოყენებით Cannizzaro რეაქციები. ამ რეაქციაში ბენზალდეჰიდი მუშავდება 40-60% ნატრიუმის ჰიდროქსიდის ხსნარით ოთახის ტემპერატურაზე. ერთდროული დაჟანგვა და შემცირება იწვევს წარმოქმნას ბენზოის მჟავადა, შესაბამისად, ფენილმეთანოლი (ბენზილის სპირტი):
ქიმიური თვისებები . კარბოქსილის მჟავები უფრო ძლიერი მჟავებია, ვიდრე ალკოჰოლი, ვინაიდან წყალბადის ატომმა კარბოქსილის ჯგუფში გაზარდა მობილურობა CO ჯგუფის გავლენის გამო. წყალხსნარში კარბოქსილის მჟავები იშლება: />
RCOOH ![]() RCOO - + H +
RCOO - + H +
თუმცა, ნახშირბადის მოლეკულების კოვალენტური ბუნების გამო მჟავებს, ზემოაღნიშნული დისოციაციის წონასწორობა საკმარისიაძლიერად გადავიდა მარცხნივ. ამრიგად, კარბოქსილის მჟავები ისინი ზოგადად სუსტი მჟავებია. მაგალითად, ეთანი (ძმარა)მჟავას ახასიათებს დისოციაციის მუდმივი K a = 1.7*10 -5./>
კარბოქსილის მჟავას მოლეკულაში არსებული შემცვლელები ძლიერად მოქმედებს მის მჟავიანობაზე ინდუქციური ეფექტი. შემცვლელები, როგორიცაა ქლორი ან ფენილის რადიკალი, იზიდავს ელექტრონის სიმკვრივეს საკუთარ თავზე და, შესაბამისად, იწვევს უარყოფით ინდუქციურ ეფექტს (-/). კარბოქსილის წყალბადის ატომიდან ელექტრონის სიმკვრივის მოშორება იწვევს კარბოქსილის მჟავიანობის მატებას. მჟავები. ამის საპირისპიროდ, შემცვლელებს, როგორიცაა ალკილის ჯგუფები, აქვთ ელექტრონის დონაციის თვისებები და ქმნიან დადებით ინდუქციურ ეფექტს, +I. ისინი ამცირებენ მჟავიანობას. შემცვლელების გავლენა კარბოქსილის მჟავების მჟავიანობაზეაშკარად ვლინდება დისოციაციის მუდმივების მნიშვნელობებშიკ ა ზოგიერთი მჟავისთვის. გარდა ამისა, მჟავას სიძლიერეგავლენას ახდენს კონიუგირებული მრავალჯერადი ბმის არსებობა.
|
კარბოქსილის მჟავების ფორმულაკ ა |
|
პროპიონური CH 3 CH 2 COOH 1.3 * 10 -5 |
|
ზეთი CH 3 CH 2 CH 2 COOH 1.5 * 10 -5 |
|
ძმარმჟავა CH 3 COOH 1.7 * 10 -5 |
|
Crotonic CH 3 - CH \u003d CH - COOH 2.0 * 10 -5 |
|
ვინილაცეტატური CH 2 \u003d CH-CH 2 COOH 3.8 * 10 -5 |
|
აკრილის CH 2 \u003d CH-COOH 5.6 * 10 -5 |
|
ფორმული HCOOH 6.1 * 10 -4 |
|
ბენზოური C 6 H 5 COOH 1.4 * 10 -4 |
|
ქლოროაციური CH 2 ClCOOH 2.2 * 10 -3 |
|
ტეტრონი CH 3 - C ≡ C - COOH 1.3 * 10 -3 |
|
დიქლოროაციური CHCl 2 COOH 5.6*10 -2 |
|
Oxalic HOOC - COOH 5.9 * 10 -2 |
|
ტრიქლოროცეტიკიCCl 3 COOH 2.2*10 -1 |
ატომების ურთიერთგავლენა დიკარბოქსილის მჟავების მოლეკულებში იწვევს იმ ფაქტს, რომ ისინი უფრო ძლიერია, ვიდრე მონობაზური მჟავები.
2. მარილის ფორმირება. კარბოქსილის მჟავებს აქვთ ჩვეულებრივი მჟავების ყველა თვისება. ისინი რეაგირებენ აქტიურ ლითონებთან, ძირითად ოქსიდებთან, ფუძეებთან და სუსტი მჟავების მარილებთან:
2 RCOOH + M გ → (RCOO) 2 მგ + H 2,
2 RCOOH + CaO → (RCOO) 2 Ca + H 2 O,
RCOOH+ NaOH → RCOONa+ H 2 O,
RCOOH+ NaHCO 3 → RCOONa+ H 2 O + CO 2.
კარბოქსილის მჟავები სუსტია, ამიტომ ძლიერი მინერალური მჟავები ანაცვლებს მათ შესაბამისი მარილებისგან:
CH 3 კოონა + HCl→ CH 3 COOH + NaCl.
წყალხსნარებში კარბოქსილის მჟავების მარილები ჰიდროლიზდება:
CH 3 SOOK + H 2 O ![]() CH 3 COOH + CON.
CH 3 COOH + CON.
კარბოქსილის მჟავებსა და მინერალურ მჟავებს შორის განსხვავება მდგომარეობს რიგი ფუნქციური წარმოებულების წარმოქმნის შესაძლებლობაში.
3 . კარბოქსილის მჟავების ფუნქციური წარმოებულების ფორმირება. კარბოქსილის მჟავებში OH ჯგუფის სხვადასხვა ჯგუფებით ჩანაცვლებისას (/>X ) წარმოიქმნება მჟავების ფუნქციური წარმოებულები მქონე ზოგადი ფორმულა R-CO-X; აქ რ ნიშნავს ალკილის ან არილის ჯგუფს. მიუხედავად იმისა, რომ ნიტრილებს აქვთ განსხვავებული ზოგადი ფორმულა ( R-CN ), ისინი ჩვეულებრივ ასევე განიხილება კარბოქსილის მჟავების წარმოებულებად, რადგან მათი მიღება შესაძლებელია ამ მჟავებისგან.
მჟავა ქლორიდები მზადდება ფოსფორის ქლორიდის მოქმედებით ( V) მჟავებისთვის:
R-CO-OH + RS l 5 → R-CO- Cl+ ROS l 3 + HCl.
|
კავშირის მაგალითები |
|
მჟავა
ეთანოინის (ძმაროვანი) ბენზოინის მჟავა მჟავა ქლორიდი
ეთანოლის ქლორიდი ბენზოილ ქლორიდი (აცეტილ ქლორიდი) მჟავა ანჰიდრიდი
ეთანის (ძმური) ბენზოური ანჰიდრიტი ანჰიდრიტი ესტერი
ეთილის ეთანოატი (ეთილის აცეტატი) მეთილის ბენზოატი ამიდი ეთანამიდი (აცეტამიდი) ბენზამიდი ნიტრილი ეთანნიტრილი ბენზონიტრილი (აცეტონიტრილი) |
ანჰიდრიდები წარმოიქმნება კარბოქსილის მჟავებისგან წყლის მოცილების აგენტების მოქმედებით:
2 R - CO - OH + P 2 O 5 → (R - CO -) 2 O + 2HPO 3.
ეთერები წარმოიქმნება მჟავას ალკოჰოლთან გაცხელებით გოგირდმჟავას თანდასწრებით (შექცევადი ესტერიფიკაციის რეაქცია):
დადგენილია ესტერიფიკაციის რეაქციის მექანიზმი „ტეგირებული ატომის“ მეთოდით.
ეთერების მიღება ასევე შესაძლებელია მჟავა ქლორიდების და ტუტე ლითონის ალკოჰოლატების რეაქციის შედეგად:
R-CO-Cl + Na-O-R' → R-CO-OR' + NaCl.
კარბოქსილის მჟავას ქლორიდების რეაქცია ამიაკთან იწვევს ამიდების წარმოქმნას:
CH 3 -CO-C l + CH 3 → CH 3 -CO-CH 2 + HCl.
გარდა ამისა, ამიდების მიღება შესაძლებელია კარბოქსილის მჟავების ამონიუმის მარილების გაცხელებით:
როდესაც ამიდები თბება დეჰიდრატაციის აგენტების თანდასწრებით, ისინი დეჰიდრატდებიან ნიტრილების წარმოქმნით:
| R 2 0 5 | ||
| CH 3 - CO - NH 2 |
→ |
CH 3 - C ≡ N + H 2 O |
ქვედა მჟავების ფუნქციური წარმოებულები არის აქროლადი სითხეები. ყველა მათგანი ადვილად ჰიდროლიზდება ორიგინალური მჟავის წარმოქმნით:
R-CO-X + H 2 O → R-CO-OH + HX.
მჟავე გარემოში ეს რეაქციები შეიძლება იყოს შექცევადი. ტუტე გარემოში ჰიდროლიზი შეუქცევადია და იწვევს კარბოქსილის მჟავების მარილების წარმოქმნას, მაგალითად:
R-CO-OR'+ NaOH → R-CO-ONa + R'OH.
4 . კარბოქსილის მჟავების მთელი რიგი თვისებები განპირობებულია ნახშირწყალბადის რადიკალის არსებობით. ამრიგად, წითელი ფოსფორის თანდასწრებით მჟავებზე ჰალოგენების მოქმედებით წარმოიქმნება ჰალოგენით შემცვლელი მჟავები, ხოლო წყალბადის ატომი კარბოქსილის ჯგუფის მიმდებარე ნახშირბადის ატომში (ა-ატომი) იცვლება ჰალოგენით:
| რ კრ | ||
|
CH 3 -CH 2 -COOH + Br 2 |
→ |
CH 3 -SNBr-COOH + HBr |
უჯერი კარბოქსილის მჟავებს შეუძლიათ დამატების რეაქციები:
CH 2 \u003d CH-COOH + H 2 → CH 3 -CH 2 -COOH,
CH 2 \u003d CH-COOH + C l 2 → CH 2 C l -CHS l -COOH,
CH 2 \u003d CH-COOH + HCl → CH 2 C l -CH 2 -COOH,
CH 2 \u003d CH-COOH + H 2 O → BUT-CH 2 -CH 2 -COOH,
ბოლო ორი რეაქცია მიმდინარეობს მარკოვნიკოვის მმართველობის წინააღმდეგ.
უჯერი კარბოქსილის მჟავებს და მათ წარმოებულებს შეუძლიათ პოლიმერიზაციის რეაქციები.

5 . კარბოქსილის მჟავების რედოქსული რეაქციები./>
კარბოქსილის მჟავები შემცირების აგენტების მოქმედებით კატალიზატორების თანდასწრებით შეიძლება გარდაიქმნას ალდეჰიდებად, სპირტებად და ნახშირწყალბადებადაც კი:
ჭიანჭველა მჟავას HCOOH-ს აქვს მრავალი მახასიათებელი, რადგან ის შეიცავს ალდეჰიდის ჯგუფს:

ჭიანჭველა მჟავა არის ძლიერი შემცირების აგენტი და ადვილად იჟანგება CO2-მდე. ის აძლევს ვერცხლის სარკის რეაქცია:
HCOOH + 2OH → 2Ag + (NH 4) 2 CO 3 + 2NH 3 + H 2 O,
ან გამარტივებული ფორმით:
C H 3 HCOOH + Ag 2 O → 2Ag + CO 2 + H 2 O.
გარდა ამისა, ჭიანჭველა მჟავა იჟანგება ქლორით:
HCOOH + Cl 2 → CO 2 + 2 HCl.
ჟანგბადის ატმოსფეროში კარბოქსილის მჟავები იჟანგება CO 2 და H 2 O :
CH 3 COOH + 2O 2 → 2CO 2 + 2H 2 O.
6. რეაქციები დეკარბოქსილაცია. გაჯერებული შეუცვლელი მონოკარბოქსილის მჟავები მაღალი სიმტკიცის გამო C-C კავშირებიგაცხელებისას ისინი ძნელად დეკარბოქსილირდება. ამისათვის საჭიროა კარბოქსილის მჟავას ტუტე ლითონის მარილის შერწყმა ტუტესთან: />
ნახშირწყალბადის რადიკალში ელექტრონის შემომტანი შემცვლელების გამოჩენა ხელს უწყობს დეკარბოქსილირების რეაქციები:
ორფუძიანი კარბოქსილის მჟავები ადვილად იშლება CO 2 გაცხელებისას:
1. ჰიდროლიზი(მჟავე და ტუტე)
ის ხდება ყველაზე მძიმე პირობებში და ყველა მჟავას წარმოებულებისგან განსხვავებით ერთ ან ორ ეტაპად, შუალედური ნაერთებია ამიდები. ნიტრილისა და წყლის თანაბარი თანაფარდობით, რეაქცია შეიძლება შეჩერდეს ამიდის წარმოქმნის ეტაპზე. ჩვეულებრივ რეაქცია მიმდინარეობს წყლის სიჭარბით, მიიღება კარბოქსილის მჟავები (მჟავა ჰიდროლიზი) ან მათი მარილები (ტუტე ჰიდროლიზი) და ამიაკი.
ა) მჟავა ჰიდროლიზი
ბ) ტუტე ჰიდროლიზი
2. ალკოჰოლიზი ნიტრილები- ეთერების სინთეზი. რეაქცია ორ ეტაპად მიმდინარეობს არასტაბილური იმინო ეთერების წარმოქმნით, რომელთა ჰიდროლიზი იწვევს ეთერებს.

3. ნიტრილების აღდგენა- პირველადი ამინების სინთეზი.
![]()
საკონტროლო კითხვები თავისთვის "მონონის ძირითადი კარბოქსი მჟავები და მათი ფუნქციური წარმოებულები"
1. დაწერეთ მჟავების სტრუქტურული ფორმულები: ა) პროპიონური; ბ) ზეთი; გ) -მეთილბუტირი; დ) ვალერიანა; ე) კაპრონი. დაასახელეთ ისინი საერთაშორისო ნომენკლატურის მიხედვით.
2. მიეცით მჟავების სტრუქტურული ფორმულები: ა) დიმეთილპროპანური; ბ) 3-მეთილბუტანური; გ) 4-მეთილ-2-ეთილპენტანური; დ) 2,2,3-ტრიმეთილბუტანური; ე) 3,5-დიმეთილ-4-ეთილჰექსანური. მიეცით ამ ნაერთებს სხვა სახელები.
3. როგორი სტრუქტურა აქვთ შემდეგ მჟავებს: ა) აკრილის; ბ) კროტონული; გ) ვინილის ძმარმჟავა? დაასახელეთ ისინი საერთაშორისო ნომენკლატურის მიხედვით. რისთვისაც შესაძლებელია მჟავა ცის - და ტრანსი- იზომერიზმი?
4. ატომების რომელ ჯგუფს უწოდებენ მჟავას ნარჩენს ან აცილს? მიეცით შემდეგი მჟავების შესაბამისი აცილები: ა) ფორმიანი; ბ) ძმარმჟავა; გ) პროპიონური; დ) ზეთი. დაასახელეთ ისინი.
5. ახსენით, რატომ ადუღდება ძმარმჟავა ეთილის სპირტზე მაღალ ტემპერატურაზე (შესაბამისად 118C და 78C) ძმარმჟავა; ბ) ქვედა მჟავები წყალში ძალიან ხსნადია; გ) ოქსილის მჟავას დნობის წერტილი მნიშვნელოვნად აღემატება ძმარმჟავას (mp 189C და 16,5C, შესაბამისად); დ) დიკარბოქსილის მჟავებს არ აქვთ დაბალი მოლეკულური წონის მონოკარბოქსილის მჟავებისთვის დამახასიათებელი უსიამოვნო სუნი.
6. ინდუქციური და მეზომერული ეფექტების გამოყენებით ახსენით კარბოქსილის ჯგუფის მოქმედება ნახშირწყალბადების ნარჩენზე მჟავებში: ა) პროპიონურ; ბ) აკრილის; გ) ვინილის ძმარმჟავა. მიუთითეთ რადიკალში ყველაზე აქტიური წყალბადის ატომები, მონიშნეთ -ელექტრონული სიმკვრივის განაწილება წილადი მუხტებით.
7. ახსენით მჟავიანობის ცვლილებები ქვემოთ მოცემულ რიგებში:

8. თითოეულ წყვილში რომელი მჟავაა უფრო ძლიერი და რატომ: ა) ფორმული და ძმარმჟავა; ბ) ძმარმჟავა და ტრიმეთილაციტური; გ) -ქლორბუტირი და -ქლორბუტირი; დ) პროპიონური და აკრილის.
9. დაწერეთ პროპიონის მჟავას რეაქციის განტოლებები მითითებული რეაგენტებით: ა)Zn;ბ) NaOH; გ) NaHCO 3 ; დ) NH 4 OH; ე) Ca(OH) 2 . პროპიონის მჟავას რა თვისება ვლინდება ამ რეაქციებში? დაასახელეთ მიღებული ნაერთები. ჩამოთვლილი რეაქციებიდან რომელი გამოიყენება ორგანულ ნაერთებში კარბოქსილის ჯგუფის ხარისხობრივი გამოსავლენად?
10. დაწერეთ პროპიონის მჟავას მეთილის სპირტით ესტერიფიკაციის სქემა გოგირდმჟავას თანდასწრებით. მოიტანეთ მექანიზმი.
11. მიეცით ეთილის პროპიონატის მჟავა და ტუტე ჰიდროლიზის სქემები. ახსენით, რატომ ახდენენ ტუტეები მხოლოდ ეთერების ჰიდროლიზს, მაგრამ არა მათ წარმოქმნას.
12. დაწერეთ რეაქციის სქემები:
![]()
დაასახელეთ პროდუქტები. რა მოხდება, თუ წარმოქმნილი ნაერთები დამუშავდება ეთილის სპირტით, დიმეთილამინით? მიეცით ბოლო რეაქციების განტოლებები, განიხილეთ ერთ-ერთი მათგანის მექანიზმი.
13. დაწერეთ ნატრიუმის აცეტატის რეაქციის სქემა და მექანიზმი აცეტილქლორიდთან, პროპიონილ ქლორიდთან. რა ხდება, როდესაც ძმარმჟავას ანჰიდრიდი თბება პროპილ სპირტით? მიეცით ამ ტრანსფორმაციის სქემა და მექანიზმი.
14. დაასახელეთ ნაერთები, რომლებიც წარმოადგენენ შემდეგი რეაქციების პროდუქტებს:
![]()
შეადარეთ პროდუქტების ძირითადი თვისებები ორიგინალურ ამინებს.
15. რა ქიმიური პროცესიაცილირებას ეძახიან? მოიყვანეთ N- და O-აცილაციის რეაქციების მაგალითები. შეადარეთ შემდეგი ნაერთების აცილირების უნარი: ა) CH 3 CH 2 COOH; ბ) CH 3 CH 2 COCl; გ) CH 3 CH 2 SOOSH 3 ; დ) (CH 3 CH 2 CO) 2 O; ე) CH 3 CH 2 CONH 2 . მჟავების რომელი ფუნქციური წარმოებულებია ყველაზე ძლიერი აცილება?
16. დაწერეთ ბუტირიუმის მჟავას წარმოებულების ჰიდროლიზის სქემა: ა) მჟავას ქლორიდი; ბ) ანჰიდრიდი; გ) ესტერი; დ) ამიდი. ახსენით მჟავებისა და ფუძეების კატალიზური მოქმედება ამ პროცესში.
17. რა ნაერთები წარმოიქმნება ეთილის აცეტატზე შემდეგი რეაგენტების მოქმედებით: ა)ჰ 2 ის + ); ბ) ჰ 2 O (NaOH); გ) CH 3 ის ნ + ); დ) CH 3 CH 2 CH 2 OH (კატ. RO); ე) NH 3 , ტ ; ე) LiAlH 4 (ეთერი), შემდეგ ჰ 2 ო?მიეცით სრული რეაქციის განტოლებები.
18. შეადარეთ ნაერთების ძირითადი და მჟავე თვისებები: ა) ეთილამინი; ბ) აცეტამიდი; v) N,N-დიმეთიაცეტამიდი. მიეცით ახსნა განსხვავებების შესახებ. დაწერეთ ამ ნაერთების რეაქციები HClეთერში და NaNH 2 ვ NH 3 თუ არის ურთიერთქმედება.
19. დაასახელეთ ბუტირიუმის მჟავის ამიდისგან წარმოქმნილი ნაერთები შემდეგი რეაგენტებით: ა) ჰ 2 ის + ); ბ) ძმ 2 +KOH; გ) LiAlH 4 (ეთერი), შემდეგ ჰ 2 O; დ) პ 2 ო 5 , ტ ; ე) HNO 2 (ჰ 2 O).
20. დაწერეთ იზობუტირმჟავას ნიტრილის ურთიერთქმედების სქემები მითითებულ რეაგენტებთან: ა) ჰ 2 ის + , ტ ; ბ) CH 3 CH 2 MgBr შემდეგ H 2 O; გ) LiAlH 4 . დაასახელეთ რეაქციის პროდუქტები.
21. დაწერეთ აკრილის მჟავას რეაქციები შემდეგ ნაერთებთან. : ა)ნა 2 CO 3 ; ბ) CH 3 CH 2 ის ნ + ); გ) SOCl 2 ; დ) HBr; ე) ძმ 2 . მიეცით რეაქციის მექანიზმი HBr.
22. ნაერთების თითოეული წყვილისთვის მიეცით ქიმიური რეაქციაგანასხვავოთ ეს ნაერთები: ა) UNUN და CH 3 COOH; ბ) CH 3 COOH და CH 3 SOOS 2 ჰ 5 ; გ) CH 3 CH 2 COOH და CH 2 =CHCOOH; დ) CH 2 =CHCOOH და HC≡ COOH; ე) CH 3 CON(CH 3 ) 2 და (CH 3 CH 2 ) 3 N; ე) CH 3 CONH 2 და CH 3 COOH 4 .
23. დაწერეთ რეაქციის განტოლებები. დაასახელეთ წყარო და დანიშნულების ნაერთები:

24. დაასახელეთ მჟავები, რომლებიც წარმოადგენენ შემდეგი რეაქციების პროდუქტებს:

25. მიუთითეთ შესაბამისი ნაერთებიდან იზობუტირმჟავას მიღების სქემები მითითებული მეთოდებით: ა) სპირტის დაჟანგვა; ბ) ნიტრილის ჰიდროლიზი; გ) გრიგნარდის რეაქცია; დ) მალონის ეთერის ალკილაცია.
26. მიიღეთ პროპიონის მჟავა შემდეგი ნაერთებისგან: ა) პროპანოლ-1; ბ) პროპენი; გ) ეთილის ბრომიდი.
27. დაწერეთ პროპიონის მჟავისგან მისი წარმოებულების მიღების სქემები: ა) ნატრიუმის მარილი; ბ) კალციუმის მარილი; გ) მჟავა ქლორიდი; დ) ამიდი; ე) ნიტრილი; ე) ანჰიდრიდი; ზ) ეთილის ეთერი.
28. დაასახელეთ ნაერთები და მიეცით მათი სინთეზის სქემები შესაბამისი მჟავებიდან: ა)CH 3 CH 2 SOOSH 3 ; ბ) (SN 3 ) 2 CHCONH 2 ; გ) CH 3 CH 2 CH 2 CN.
29. შეავსეთ ტრანსფორმაციის სქემები. დაასახელეთ ყველა მიღებული ნაერთი:

30. რა რეაგენტების მოქმედებით და რა პირობებში შეიძლება განხორციელდეს ეს გარდაქმნები (დაასახელეთ ყველა ნაერთი).
1. კარბოქსილის მჟავების ანჰიდრიდები
კარბოქსილის მჟავების ანჰიდრიდები არის წყლის მოლეკულის ელიმინაციის პროდუქტები მჟავას ორი მოლეკულიდან.
1.1. კარბოქსილის ანჰიდრიდების მომზადების მეთოდები
კარბოქსილის მჟავების ანჰიდრიდები, როგორც ახლა ვნახეთ (3.1), შეიძლება მივიღოთ მჟავა ქლორიდებიდან და კარბოქსილის მჟავების მარილებიდან. გარდა ამისა, მათი მიღება შესაძლებელია აცილის ქლორიდებიდან და კარბოქსილის მჟავებიდან პირიდინის თანდასწრებით:
აცილის ქლორიდის მჟავა პირიდინის ანჰიდრიდი პირიდინიუმის ქლორიდი
ბევრი კარბოქსილის მჟავის ანჰიდრიდები წარმოიქმნება შესაბამისი კარბოქსილის მჟავების გაცხელებით, ხშირად დეჰიდრატაციის აგენტების გამოყენებით. ასე რომ, ძმარმჟავას ანჰიდრიდი მიიღება კონცენტრირებული გოგირდის მჟავით გაცხელებით:
 (28)
(28)
ძმარმჟავას ანჰიდრიდი
იაფი ძმარმჟავას ანჰიდრიდი ზოგჯერ გამოიყენება როგორც დეჰიდრატაციის საშუალება:
სავარჯიშო 19. ბენზოის ანჰიდრიდი შეიძლება მომზადდეს ბენზოილის ქლორიდის ორ მოლ ეკვივალენტს წყლის ერთი მოლური ექვივალენტის დამატებით. დაწერეთ ეს რეაქცია.
დიკარბოქსილის მჟავების ციკლური ანჰიდრიდები ხშირად წარმოიქმნება მათი უბრალოდ გაცხელებით:
 (31)
(31)
სუქცინის მჟავა სუქცინის ანჰიდრიდი
მალეინის ანჰიდრიდის წარმოების სამრეწველო მეთოდი არის ბენზოლის ან 2-ბუტენის დაჟანგვა ჰაერით:
 (32)
(32)
ფტალიუმის ანჰიდრიდი წარმოიქმნება ინდუსტრიულად ნაფტალინის ან ო-ქსილენის დაჟანგვით:
 (33)
(33)
ძმარმჟავას ანჰიდრიდი წარმოიქმნება ინდუსტრიულად აცეტალდეჰიდის დაჟანგვით ატმოსფერული ჟანგბადით სპილენძ-კობალტის კატალიზატორის თანდასწრებით:
სავარჯიშო 20. მალეინის მჟავა გარდაიქმნება მალეინის ანჰიდრიდად 200°C ტემპერატურაზე მალეინის ანჰიდრიდის მისაღებად ფუმარინის მჟავასაგან საჭიროა გაცილებით მაღალი ტემპერატურა. რა ხსნის ამას? დაწერეთ შესაბამისი რეაქციები.
სავარჯიშო 21. დაწერეთ პროპიონის ანჰიდრიდის რეაქციები ა) წყალთან, ბ) ეთანოლთან, გ) ამიაკთან, დ) ეთილამინთან და აღწერეთ მათი მექანიზმი.
სავარჯიშო 22. რა ტექნიკური მეთოდები არსებობს ძმარმჟავას ანჰიდრიდის მისაღებად? რა არის მისი სამრეწველო გამოყენება?
სავარჯიშო 23. სრული რეაქციები

![]()
1.2. კარბოქსილის მჟავების ანჰიდრიდების რეაქციები
კარბოქსილის მჟავების ანჰიდრიდები შედიან იმავე რეაქციებში, როგორც მჟავა ქლორიდები:
 (35)
(35)
მეთილის აცეტატი
 (M 6)
(M 6)
 (37)
(37)
აცეტამიდი
აცეტილის ჯგუფების შემცველი ნაერთები ყველაზე ხშირად მზადდება ძმარმჟავას ანჰიდრიდისგან: ის არის იაფი, ადვილად ხელმისაწვდომი, არც თუ ისე აქროლადი და არ გამოყოფს კოროზიულ HCl-ს.
 (38)
(38)
ძმარმჟავას ანჰიდრიდი ნილინ აცეტანილიდი

 (M 7)
(M 7)
სავარჯიშო 24. დაწერეთ აცეტანჰიდრიდის (ა) რეაქციები ანილინთან და (ბ) სალიცილის მჟავასთან და აღწერეთ მათი მექანიზმი.
ფორმალურად, კეტნები შეიძლება ჩაითვალოს მონოკარბოქსილის მჟავების შიდა ანჰიდრიდებად RCH=C=O. უმარტივეს კეტენს CH 2 \u003d C \u003d O უბრალოდ კეტენი ეწოდება.
კეტენი მიიღება მჟავების მაღალი ტემპერატურის გაუწყლოებით
 (39)
(39)
ან აცეტონის პიროლიზი
კეტენი შედის დამატებით რეაქციებში იმავე პროდუქტების წარმოქმნით, რომლებიც შეიძლება მიღებულ იქნას ძმარმჟავას ანჰიდრიდისა და აცეტილ ქლორიდისგან:
მაგ. 25. დაწერეთ კეტენის რეაქციები ა) წყალთან, ბ) 1-პროპანოლთან, გ) ფენოლთან, დ) მეთილამინთან, ე) ანილინთან.
კეტენი ადვილად დიმერიზდება დიკეტენად:
დიკეტენი შედის დამატებით რეაქციებში სქემის მიხედვით:
აცეტოაცეტატური ესტერი
მაგ. 26. დაწერეთ დიკეტენის რეაქციები ა) წყალთან, ბ) მატანოლთან, გ) ამიაკთან, დ) ანილინთან.
3. ნიტრილები
ნიტრილები დასახელებულია სხვადასხვა გზით:
CH 3 CN CH 2 \u003d CHCN PhCN NC (CH 2) 4 CN
ეთანენიტრილი პროპენნიტრილი ბენზოლეკარბონიტრილი ადიპონიტრილი
(აცეტონიტრილი) (აკრილონიტრილი) (ბენზონიტრილი)
3.1. ნიტრილების მიღების მეთოდები
3.1.1. ნიტრილების მიღება ამიდების დეჰიდრატაციით
ამიდების დეჰიდრატაცია, რომელიც წინა ნაწილში განვიხილეთ, შეიძლება გახდეს კარბოქსილის მჟავის ამ მჟავის ნიტრილად გარდაქმნის ჯაჭვის ბოლო ნაბიჯი:
ყველა ეს რეაქცია ხშირად გაერთიანებულია ერთ პროცესში, კარბოქსილის მჟავისა და ამიაკის ნარევი ალუმინის გავლით 500 o C ტემპერატურაზე:
სავარჯიშო 46. დაწერეთ ადიპინის მჟავიდან ადიპონიტრილის მიღების სამრეწველო მეთოდის რეაქცია.
3.1.2. ნიტრილების მიღება ნახშირწყალბადების ოქსიდაციური ამმონოლიზით
ნახშირწყალბადების დაჟანგვის შესწავლისას ვნახეთ, რომ ჰიდროციანმჟავა (ჭიანჭველა მჟავა ნიტრილი) და სხვა მჟავების ნიტრილები მიიღება შესაბამისი ნახშირწყალბადების ჟანგვითი ამონოლიზით სქემის მიხედვით:
სავარჯიშო 47. დაწერეთ რეაქციები ა) აკრილონიტრილის, ბ) ბენზონიტრილის, გ) აცეტონიტრილის და დ) ტერეფტალის მჟავას ნიტრილის მისაღებად შესაბამისი ნახშირწყალბადების ოქსიდაციური მონოლიზით.
3.1.3. ნიტრილების მიღება კოლბის რეაქციით
როდესაც ჰალოკარბონები ურთიერთქმედებენ კალიუმის ციანიდთან წყალხსნარში ეთანოლში, ნიტრილები წარმოიქმნება S N 2 მექანიზმით:
ვინაიდან ციანიდის ანიონი არის ამბიდენტური იონი, იზონიტრილები წარმოიქმნება როგორც ქვეპროდუქტი, რომლებიც ამოღებულია სარეაქციო ნარევის განზავებული მარილმჟავით შერყევის შედეგად.
სავარჯიშო 48. დაწერეთ რეაქციები ეთილენიდან პროპიონიტრილის, ბ) პროპილენიდან ბუტირონიტრილის, გ) ეთილენისგან სუქცინის დინიტრილის მისაღებად, პროპილენიდან ვინილძმარმჟავას ნიტრილის, ე) ტოლუოლისგან ფენილძმარმჟავას ნიტრილის, ე) ფენილ ძმარმჟავას ნიტრილის მისაღებად. მჟავა ნიტრილი ტოლუოლიდან, (ვ) ადიპინის მჟავა დინიტრილი აცეტილენიდან.
სავარჯიშო 49. სრული რეაქციები:
(ა) (ბ) 
3.2. ნიტრილების რეაქციები
3.2.1. ნიტრილების ჰიდროგენიზაცია
ნიტრილები ადვილად ჰიდროგენდება ამინებში. ჰიდროგენიზაცია ხორციელდება ან წყალბადით იზოლაციის დროს (C 2 H 5 OH + Na) ან კატალიზურად:
სავარჯიშო 50. დაწერეთ (ა) პროპიონიტრილის, (ბ) ბუტირონიტრილის, (გ) სუქცინის მჟავას დინიტრილის, (დ) ვინილძმარმჟავას ნიტრილის, (ე) ფენილძმარმჟავას ნიტრილის, (ვ) ადიპინის მჟავას დინიტრილის ჰიდროგენაციის რეაქციები.
3.2.2. ნიტრილების ჰიდროლიზი
ნუკლეოფილური ჩანაცვლების რეაქციით ალკილის ჰალოიდებიდან და მეტალის ციანიდებიდან მიღებული ნიტრილები კარგი საწყისი პროდუქტია კარბოქსილის მჟავების მოსამზადებლად. ამისათვის ისინი ექვემდებარებიან ჰიდროლიზს მჟავების ან ფუძეების თანდასწრებით:

სავარჯიშო 51. რა მჟავები წარმოიქმნება შემდეგი ნიტრილების ჰიდროლიზის დროს:
(ა) პროპიონიტრილი, (ბ) ბუტირონიტრილი, (გ) სუქცინის მჟავა დინიტრილი, (დ) ვინილძმარმჟავას ნიტრილი, (ე) ფენილძმარმჟავას ნიტრილი, (ვ) ადიპინის მჟავა დინიტრილი.
ამ სქემის მიხედვით, ფენილძმარმჟავა მიიღება ხელმისაწვდომი ბენზილის ქლორიდიდან:
 (87)
(87)
სავარჯიშო 52. შემოგვთავაზეთ ტოლუენიდან დაწყებული ფენილძმარმჟავას წარმოების სქემა. აღწერეთ შესაბამისი რეაქციების მექანიზმები.
მალონის მჟავა ძირითადად მიიღება ქლოროძმარმჟავისგან სქემის მიხედვით:
სავარჯიშო 53. ეთილენისა და სხვა საჭირო რეაგენტებიდან გამომდინარე, შემოგვთავაზეთ ბუტანედიოური (საქცინის) მჟავის მიღების სქემა.
სავარჯიშო 54. შესაბამისი ჰალოკარბონების და ნიტრილების გამოყენებით, შემოგვთავაზეთ შემდეგი მჟავების მიღების სქემები: (ა) პროპიონის მჟავა ეთილენიდან, (ბ) ბუტირის მჟავა პროპილენიდან, (გ) სუქცინის მჟავა ეთილენიდან, (დ) ვინილძმარმჟავა პროპილენიდან, (ე) ტოლუოლისგან ფენილძმარმჟავა, (ე) აცეტილენისგან ადიპინის მჟავა.
ხელმისაწვდომი ციანოჰიდრინებიდან მიიღება ა-ჰიდროქსი მჟავები:
 (89)
(89)
სავარჯიშო 55. შესაბამის ალდეჰიდებსა და კეტონებზე და სხვა საჭირო რეაგენტებზე დაყრდნობით, შემოგვთავაზეთ სქემები (ა) 2-ჰიდროქსიოქსიპროპიონის მჟავისა და
ბ) 2-მეთილ-2-ჰიდროქსიპროპიონის მჟავა.
3.3. ნიტრილების ალკოჰოლიზი
ნიტრილები რეაგირებენ წყალბადის ქლორიდთან იმინო ქლორიდების წარმოქმნით:
 (90)
(90)
მინოქლორიდი
წყალბადის ქლორიდის მოქმედება ალკოჰოლში ნიტრილებზე იწვევს იმინოესტერის ჰიდროქლორიდების წარმოქმნას, რომელთა შემდგომი ჰიდროლიზი იძლევა ეთერებს:
მეთილის მეთაკრილატი ინდუსტრიულად მიიღება აცეტონისგან ციანოჰიდრინის მეშვეობით:
აცეტონი აცეტონი ციანოჰიდრინი მეთილის მეთაკრილატი
მეთილის მეთაკრილატის პოლიმერი - პოლიმეთილ მეთაკრილატი გამოიყენება უსაფრთხოების სათვალეების (პლექსიგლასის) წარმოებაში.
მაგ. 56. რა პროდუქტი წარმოიქმნება კალიუმის ციანიდის, ეთანოლის თანმიმდევრული მოქმედების შედეგად წყალბადის ქლორიდის და ბოლოს, წყლის ბენზილქლორიდზე? დაწერეთ შესაბამისი რეაქციები.
მაგ. 57. რა პროდუქტი წარმოიქმნება ჰიდროციანმჟავას აცეტალდეჰიდზე, შემდეგ კი მეთანოლზე გოგირდმჟავას თანმიმდევრული მოქმედების შედეგად? დაწერეთ შესაბამისი რეაქციები.
4. ციანამიდი
დიდი პრაქტიკული მნიშვნელობა აქვს ჰიდროციანმჟავას ამიდს - ციანამიდს. ინდუსტრიაში მას იღებენ კალციუმის კარბიდიდან და აზოტიდან 1000-1100 C ტემპერატურაზე ან 650-800 C ტემპერატურაზე დაახლოებით 10% კალციუმის ქლორიდის თანდასწრებით.
კალციუმის ციანამიდი
კალციუმის ციანამიდის და ნახშირბადის ნაზავი პირდაპირ გამოიყენება სასუქად. როდესაც გოგირდის მჟავა მოქმედებს კალციუმის ციანამიდზე, მიიღება ციანამიდი:
მყარ მდგომარეობაში და ხსნარებში ციანამიდი წონასწორობაშია კარბოდიიმიდთან:
ციანამიდის კარბოდიიმიდი
შარდოვანა მიიღება ციანამიდის ნაწილობრივი ჰიდროლიზით:
 (94)
(94)
ციანამიდზე წყალბადის სულფიდის მოქმედებით წარმოიქმნება თიოურა:
 (95)
(95)
თიოურეა
მისი ურთიერთქმედება ამიაკთან იწვევს გუანიდინის წარმოქმნას:
 (96)
(96)
გუანიდინი
გაცხელებისას ციანამიდი იქცევა მელამინად.
1. ჰიდროლიზი (მჟავე და ტუტე)
ის ხდება ყველაზე მძიმე პირობებში და ყველა მჟავას წარმოებულებისგან განსხვავებით ერთ ან ორ ეტაპად, შუალედური ნაერთებია ამიდები. ნიტრილისა და წყლის თანაბარი თანაფარდობით, რეაქცია შეიძლება შეჩერდეს ამიდის წარმოქმნის ეტაპზე. ჩვეულებრივ რეაქცია მიმდინარეობს წყლის სიჭარბით, მიიღება კარბოქსილის მჟავები (მჟავა ჰიდროლიზი) ან მათი მარილები (ტუტე ჰიდროლიზი) და ამიაკი.
ა) მჟავა ჰიდროლიზი








ბ) ტუტე ჰიდროლიზი
2. ნიტრილების ალკოჰოლიზი – ეთერების სინთეზი. რეაქცია ორ ეტაპად მიმდინარეობს არასტაბილური იმინოეთერების წარმოქმნით, რომელთა ჰიდროლიზი იწვევს ეთერებს.

3. ნიტრილების აღდგენა – პირველადი ამინების სინთეზი

საკონტროლო კითხვები თავისთვის "მონონის ძირითადი კარბოქსი მჟავები და მათი ფუნქციური წარმოებულები"
- 1. დაწერეთ მჟავების სტრუქტურული ფორმულები: ა) პროპიონური; ბ) ზეთი; გ) -მეთილბუტირიკი; დ) ვალერიანა; ე) კაპრონი. დაასახელეთ ისინი საერთაშორისო ნომენკლატურის მიხედვით.
- 2. მიეცით მჟავების სტრუქტურული ფორმულები: ა) დიმეთილპროპანური; ბ) 3-მეთილბუტანური; გ) 4-მეთილ-2-ეთილპენტანური; დ) 2,2,3-ტრიმეთილბუტანური; ე) 3,5-დიმეთილ-4-ეთილჰექსანური. მიეცით ამ ნაერთებს სხვა სახელები.
- 3. როგორი სტრუქტურა აქვთ შემდეგ მჟავებს: ა) აკრილის; ბ) კროტონული; გ) ვინილის ძმარმჟავა? დაასახელეთ ისინი საერთაშორისო ნომენკლატურის მიხედვით. რომელი მჟავისთვის არის შესაძლებელი ცის- და ტრანს-იზომერიზმი?
- 4. ატომების რომელ ჯგუფს უწოდებენ მჟავას ნარჩენს ან აცილს? მიეცით შემდეგი მჟავების შესაბამისი აცილები: ა) ფორმიანი; ბ) ძმარმჟავა; გ) პროპიონური; დ) ზეთი. დაასახელეთ ისინი.
- 5. ახსენით, რატომ: ა) ძმარმჟავა ადუღდება ეთილის სპირტზე მაღალ ტემპერატურაზე (შესაბამისად 118C და 78C bp); ბ) ქვედა მჟავები წყალში ძალიან ხსნადია; გ) ოქსილის მჟავას დნობის წერტილი მნიშვნელოვნად აღემატება ძმარმჟავას (mp 189C და 16.5C, შესაბამისად); დ) დიკარბოქსილის მჟავებს არ აქვთ დაბალი მოლეკულური წონის მონოკარბოქსილის მჟავებისთვის დამახასიათებელი უსიამოვნო სუნი.
- 6. ინდუქციური და მეზომერული ეფექტების გამოყენებით ახსენით კარბოქსილის ჯგუფის მოქმედება ნახშირწყალბადების ნარჩენზე მჟავებში: ა) პროპიონურ; ბ) აკრილის; გ) ვინილის ძმარმჟავა. მიუთითეთ რადიკალში ყველაზე აქტიური წყალბადის ატომები, მონიშნეთ -ელექტრონის სიმკვრივის განაწილება წილადი მუხტებით.
- 7. ახსენით მჟავიანობის ცვლილებები ქვემოთ მოცემულ რიგებში:

- 8. თითოეულ წყვილში რომელი მჟავაა უფრო ძლიერი და რატომ: ა) ფორმული და ძმარმჟავა; ბ) ძმარმჟავა და ტრიმეთილაციტური; გ) -ქლორბუტირი და -ქლორბუტირი; დ) პროპიონური და აკრილის.
- 9. დაწერეთ პროპიონის მჟავას რეაქციები მითითებულ რეაგენტებთან: ა) Zn; ბ) NaOH; გ) NaHCO3; დ) NH4OH; ე) Ca(OH)2. პროპიონის მჟავას რა თვისება ვლინდება ამ რეაქციებში? დაასახელეთ მიღებული ნაერთები. ჩამოთვლილი რეაქციებიდან რომელი გამოიყენება ორგანულ ნაერთებში კარბოქსილის ჯგუფის ხარისხობრივი გამოსავლენად?



































- 10. დაწერეთ პროპიონის მჟავას მეთილის სპირტით ესტერიფიკაციის სქემა გოგირდმჟავას თანდასწრებით. მოიტანეთ მექანიზმი.
- 11. მიეცით ეთილის პროპიონატის მჟავა და ტუტე ჰიდროლიზის სქემები. ახსენით, რატომ ახდენენ ტუტეები მხოლოდ ეთერების ჰიდროლიზს, მაგრამ არა მათ წარმოქმნას.
- 12. დაწერეთ რეაქციის სქემები:

დაასახელეთ პროდუქტები. რა მოხდება, თუ წარმოქმნილი ნაერთები დამუშავდება ეთილის სპირტით, დიმეთილამინით? მიეცით ბოლო რეაქციების განტოლებები, განიხილეთ ერთ-ერთი მათგანის მექანიზმი.
13. დაწერეთ ნატრიუმის აცეტატის რეაქციის სქემა და მექანიზმი აცეტილქლორიდთან, პროპიონილ ქლორიდთან. რა ხდება, როდესაც ძმარმჟავას ანჰიდრიდი თბება პროპილ სპირტით? მიეცით ამ ტრანსფორმაციის სქემა და მექანიზმი.
14. დაასახელეთ ნაერთები, რომლებიც წარმოადგენენ შემდეგი რეაქციების პროდუქტებს:

შეადარეთ პროდუქტების ძირითადი თვისებები ორიგინალურ ამინებს.
- 15. რომელ ქიმიურ პროცესს ეწოდება აცილირება? მოიყვანეთ N- და O-აცილაციის რეაქციების მაგალითები. შეადარეთ შემდეგი ნაერთების აცილირების უნარი: ა) CH3CH2COOH; ბ) CH3CH2COCl; გ) CH3CH2COOCH3; დ) (CH3CH2CO)2O; ე) CH3CH2CONH2. მჟავების რომელი ფუნქციური წარმოებულებია ყველაზე ძლიერი აცილება?
- 16. დაწერეთ ბუტირიუმის მჟავას წარმოებულების ჰიდროლიზის სქემა: ა) მჟავას ქლორიდი; ბ) ანჰიდრიდი; გ) ესტერი; დ) ამიდი. ახსენით მჟავებისა და ფუძეების კატალიზური მოქმედება ამ პროცესში.
- 17. რა ნაერთები წარმოიქმნება ეთილის აცეტატზე შემდეგი რეაგენტების მოქმედებით: ა) H2O (H+); ბ) H2O (NaOH); გ) CH3OH (H+); დ) CH3CH2CH2OH (კატ. RO); ე) NH3, t; ე) LiAlH4 (ეთერი), შემდეგ H2O? მიეცით სრული რეაქციის განტოლებები.
- 18. შეადარეთ ნაერთების ძირითადი და მჟავე თვისებები: ა) ეთილამინი; ბ) აცეტამიდი; გ) N,N-დიმეთიაცეტამიდი. მიეცით ახსნა განსხვავებების შესახებ. ჩაწერეთ ამ ნაერთების რეაქციები HCl-თან ეთერში და NaNH2-ში NH3-ში, თუ არის ურთიერთქმედება.
- 19. დაასახელეთ ბუტირის მჟავას ამიდისგან წარმოქმნილი ნაერთები შემდეგი რეაგენტებით: ა) H2O (H+); ბ) Br2+KOH; გ) LiAlH4 (ეთერი), შემდეგ H2O; დ) Р2О5, ტ; ე) HNO2 (H2O).
- 20. დაწერეთ იზობუტირმჟავას ნიტრილის ურთიერთქმედების სქემები მითითებულ რეაგენტებთან: ა) H2O, H+, t; ბ) CH3CH2MgBr, შემდეგ H2O; გ) LiAlH4. დაასახელეთ რეაქციის პროდუქტები.
- 21. დაწერეთ აკრილის მჟავას რეაქციები შემდეგ ნაერთებთან: ა) Na2CO3; ბ) CH3CH2OH (H+); გ) SOCl2; დ) HBr; ე) Br2. მიუთითეთ რეაქციის მექანიზმი HBr-თან.
- 22. ნაერთების თითოეულ წყვილზე მიეცით ქიმიური რეაქცია, რომელიც განასხვავებს ამ ნაერთებს: ა) HCOOH და CH3COOH; ბ) CH3COOH და CH3COOC2H5; გ) CH3CH2COOH და CH2=CHCOOH; დ) CH2=CHCOOH და HC?CCOOH; ე) CH3CON(CH3)2 და (CH3CH2)3N; ვ) CH3CONH2 და CH3COOHNH4.

23. დაწერეთ რეაქციის განტოლებები. დაასახელეთ წყარო და დანიშნულების ნაერთები:

24. დაასახელეთ მჟავები, რომლებიც წარმოადგენენ შემდეგი რეაქციების პროდუქტებს:

- 25. მიუთითეთ შესაბამისი ნაერთებიდან იზობუტირმჟავას მიღების სქემები მითითებული მეთოდებით: ა) სპირტის დაჟანგვა; ბ) ნიტრილის ჰიდროლიზი; გ) გრიგნარდის რეაქცია; დ) მალონის ეთერის ალკილაცია.
- 26. მიიღეთ პროპიონის მჟავა შემდეგი ნაერთებისგან: ა) პროპანოლ-1; ბ) პროპენი; გ) ეთილის ბრომიდი.
- 27. დაწერეთ პროპიონის მჟავისგან მისი წარმოებულების მიღების სქემები: ა) ნატრიუმის მარილი; ბ) კალციუმის მარილი; გ) მჟავა ქლორიდი; დ) ამიდი; ე) ნიტრილი; ე) ანჰიდრიდი; ზ) ეთილის ეთერი.
- 28. დაასახელეთ ნაერთები და მიეცით მათი სინთეზის სქემები შესაბამისი მჟავებისგან: ა) CH3CH2COOSH3; ბ) (CH3)2CHCONH2; გ) CH3CH2CH2CN.

29. შეავსეთ ტრანსფორმაციის სქემები. დაასახელეთ ყველა მიღებული ნაერთი: