Электронные представления об окислении и восстановлении. Химические реакции могут протекать без изменения или с изменением степени окисления элементов, например:

Если в первом примере (реакция нейтрализации) ни один из элементов не меняет степени окисления, то во втором - изменяется от +2 до 0 степень окисления цинка и от 0 до +2 степень окисления углерода.
Реакции, протекающие с изменением степени окисления элементов, называются окислительно-восстановительными.
Изменение степеней окисления произошло очевидно вследствие перехода двух электронов от углерода к цинку, что может быть выражено электронными уравнениями полуреакций окисления и восстановления, которые при сложении дают уравнение окислительно-восстановительной реакции:
восстановитель  окисление;
окисление;
окислитель  восстановление;
восстановление;

Элемент, отдающий электроны, называется восстановителем, в ходе реакции он окисляется, его степень окисления увеличивается.
Элемент, принимающий электроны, называется окислителем, в ходе реакции он восстанавливается, его степень окисления уменьшается.
Понятия окислитель и восстановитель распространяются также на простые и сложные вещества, содержащие соответствующие элементы. В приведенном примере восстановителем является простое вещество: углерод С, окислителем - сложное вещество: оксид цинка ZnO .
В общем случае окислительно-восстановительная реакция может быть обратимой, в результате восстановитель превращается в окислитель, а окислитель - в восстановитель:
восстановитель - ne ↔ окислитель
окислитель + ne ↔ восстановитель
Таким образом, окислительно-восстановительная реакция представляет собой неразрывное единство двух полуреакций - окисления и восстановления, причем количества электронов, отданных восстановителем и принятых окислителем равны.
Окислительно-восстановительные свойства простых и сложных веществ. Простые вещества - металлы, обладая небольшой электроотрицательностью, сравнительно легко теряют электроны, проявляя исключительно восстановительные свойства. Наиболее ярко они выражены у щелочных металлов. Для простых веществ - неметаллов с большой электроотрицательностью характерны окислительные свойства. Абсолютным окислителем является фтор, ярко выражены окислительные свойства также у кислорода (кроме реакции с фтором, где кислород играет роль восстановителя). Однако неметаллы со сравнительно небольшой электроотрицателъностью, например углерод, водород наряду с окислительными могут проявлять и восстановительные свойства, отдавая электроны более сильным окислителям.
Сложные вещества могут быть окислителями или восстановителями в зависимости от величины степени окисления элементов, входящих в их состав.
Если степень окисления элемента в данном соединении велика, он имеет возможность понизить ее, принимая электроны. Вещество в таком случае будет окислителем. Важнейшими окислителями являются: азотная кислота Н NO з и ее соли - нитраты, тетраoксид азота N 2 O 4 , соли хлорной кислоты НС1О 4 - перхлораты, перманганат калия КМпО 4 и др.
Если в состав соединения входит элемент с небольшой степенью окисления, он может ее повысить, отдавая электроны. Сложное вещество, содержащее такой элемент, будет проявлять восстановительные свойства. Важнейшими восстановителями являются аммиак N Н 3 , гидразин N 2 H 4 и его органические производные, углеводороды, спирты, амины и другие вещества.
Очевидно, если в состав соединения входит элемент с промежуточной степенью окисления, он может понизить ее, принимая электроны, или повысить, отдавая электроны. Понятия окислитель и восстановитель в этом случае становятся относительными: вещество в зависимости от свойств партнера по реакции будет проявлять либо окислительные, либо восстановительные свойства. Примером может служить пероксид водорода Н 2 О 2 , степень окисления кислорода в котором равна -1. Ее величина может уменьшиться до -2 путем присоединения одного электрона или увеличиться до 0 путем его отдачи. Поэтому при взаимодействии с энергичными восстановителями пероксид водорода ведет себя как окислитель, а в реакции с энергичными окислителями - как восстановитель.
Составление уравнений окислительно-восстановительных реакций.
Окислительно-восстановительные реакции часто выражается сложными уравнениями. Для подбора коэффициентов в них применяют два метода: метод электронных уравнений и метод электронно-ионных уравнений.
Метод электронных уравнений базируется на понятии степени окисления. Он носит универсальный характер и применим для всех типов окислительно-восстановительных реакций. Метод включает следующие операции:
1. Записывают схему реакции с указанием степени окисления элементов, например:
![]()
2. Определяют элементы, изменившие степень окисления. В данной реакции степень окисления изменили углерод и азот, у водорода и кислорода величина степени окисления осталась неизменной.
3. Составляют электронные уравнения полуреакций окисления и восстановления с соблюдением равенства масс и зарядов:

Числа электронов, отданных восстановителем и принятых окислителем должны быть равны, поэтому следует первое уравнение умножить на три, а второе - на четыре. Указанные множители являются коэффициентами для восстановителя С, окислителя HNO 3 и продуктов их превращений СО и NO :
3C + 4HNO 3 ® 3CO 2 + 4NO + Н 2 О ,
4. Коэффициенты для остальных веществ, состоящих из элементов с неизменной степенью окисления, находят из баланса соответствующих атомов в левой и правой частях уравнения. В рассмотренной реакции таким веществом является вода, перед формулой которой нужно поставить коэффициент два. Окончательное уравнение запишется в виде:
3C + 4HNO 3 ® 3CO 2 + 4NO + 2Н 2 О
Метод электронно-ионных уравнений применяют при составлении уравнений реакций, протекающих в растворах электролитов. В этом случае степень окисления не определяется, а процессы окисления и восстановления записываются для реальных ионов и молекул, находящихся в растворе.
С целью сохранения баланса масс используют частицы среды, в которой протекает реакция. В любых водных растворах это молекулы воды, в кислых - дополнительно ионы Н + и в щелочных - ионы ОН - .
Последовательность действий следующая:
1. Составляют ионную схему реакции, записывая сильные электролиты в виде ионов, газообразные, нерастворимые вещества и слабые электролиты в виде молекул:
С + Н + + NO 3 - ® CO 2 + NO + Н 2 О
2. 3аписывают электронно-ионные уравнения полуреакций окисления и восстановления.
В данной реакции в роли восстановителя выступает углерод С, который окисляясь превращается в диоксид углерода СО 2 . Для сохранения баланса масс в левую часть уравнения добавляют две молекулы Н 2 О, а в правую - четыре иона Н - . Баланс зарядов сохраняют, отнимая от левой части уравнения четыре электрона:
С + 2Н 2 О - 4е ® С O 2 + 4Н +
Окислителем служит ион NO 3 - , превращающийся в NO , Баланс масс обеспечивается в этом случае добавлением двух молекул H 2 O в правую часть уравнения и четырех ионов Н + в его левую часть. Поскольку суммарный заряд частиц в левой части уравнения равен плюс три, а в правой - нулю, к левой части необходимо добавить три электрона:
NO 3 - + 4Н + + 3е ® NO + H 2 O
3. Суммируют уравнения полуреакций, предварительно уравняв числа отданных и принятых электронов:

После сокращения подобных членов, получают ионное уравнение:
ЗС + 4H + + 4 NO 3 - ® ЗСО 2 + 4 NO + 2Н 2 О
4. Объединяют ионы в молекулы и получают итоговое молекулярное уравнение реакции:
3С + 4Н NO 3 ® 3СО 2 + 4 NO + 2Н 2 О
Сравнивая рассмотренные метода составления уравнений окислительно-восстановительных реакций, следует отметить, что оба они приводят к одинаковому конечному результату. Однако метод электронно-ионных уравнений более информативен, он оперирует не гипотетическими, а реальными ионами и молекулами, существующими в растворах электролитов. Особенно полезен он при описании электрохимических процессов.
5.2. Электрохимические системы.
Электродные потенциалы. Электрохимическими называются процессы взаимного превращения химической и электрической энергии. Эти превращения осуществляются в результате окислительно-восстановительных реакций, протекающих на границе раздела фаз между электронным и ионным проводниками. Электронный проводник, находящийся в контакте с ионным, называется электродом.
Рассмотрим электрод, состоящий из пластинки активного металла - цинка, погруженной в водный раствор сульфата цинка, диссоциирующего на ионы:
ZnSO 4 ↔ Zn 2+ SO 4 2-
Положительно заряженные катионы цинка, расположенные на поверхности пластинки, в результате взаимодействия с полярными молекулами воды отрываются от пластинки и переходят в раствор, электроны остаются в металле. Происходит процесс окисления:
Zn 0 – 2е ® Zn 2+
Одновременно протекает и обратный процесс: катионы цинка из раствора притягиваются поверхностью металла и входят в состав его кристаллической решетки. Идет процесс восстановления:
Zn 2+ +2е ® Zn 0
По мере увеличения концентрации катионов цинка в растворе скорость выхода ионов из металла уменьшается, а скорость их перехода в металл возрастает. Когда скорости этих процессов сравняются, на границе металл-электролит установится окислительно-восстановительное равновесие между металлом и его ионами, которое условились записывать как обратимый процесс восстановления:
![]()
При записи электрохимической схемы электрода его окисленную форму отделяют от восстановленной чертой: Zn +2 / Zn .
Поскольку цинк является активным металлом, равновесие процесса смещено влево, то есть в раствор переходит больше ионов, чем возвращается обратно. В результате цинковая пластинка приобретает отрицательный потенциал (рис. 5.1 а).
Те же процессы происходят и при погружении пластинки из малоактивного металла- меди в раствор сульфата меди, диссоциирующего на ионы:
Однако в этом случае металл посылает в раствор незначительное число катионов, преобладает процесс осаждения катионов на металле и равновесие смещено вправо:
![]()
Медный электрод С u 2+ /Сu приобретает положительный потенциал (рис. 5.1.).
Рисунок 5.1. Схема возникновения электродного потенциала
а) активного металла; б) малоактивного металла
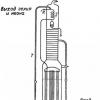
Абсолютную величину электродного потенциала измерить невозможно, поэтому измеряют ее относительно потенциала электрода сравнения, в качестве которого используют стандартный водородный электрод (рис.5.2). Он представляет собой платиновую пластинку в водном растворе серной кислоты с концентрацией ионов водорода Сн + = 1 моль/л, омываемую водородом с давлением 101,3 кПа при температуре 293К.
Платина обладает способностью адсорбировать водород и на границе
Рисунок 5.2. Схема водородного электрода
раздела фаз устанавливается равновесиемежду молекулами и ионами водорода:
2Н + + 2е ↔ Н 2
Соответствующий электродный потенциал условно принимают за нуль, Е 0 2Н + / Н2 = 0.
Стандартным электродным потенциалом металла называют разность потенциалов между данным металлом, опущенным в раствор своей соли с концентрацией ионов металла С М n + =1 моль/л при температуре 293К и стандартным водородным электродом.
Стандартный электродный потенциал является мерой окислительно-восстановительной активности системы.
С увеличением величины стандартного электродного потенциала восстановительная активность системы уменьшается, а окислительная - растет.
Так, с ростом величины стандартного электродного потенциала металлов уменьшается восстановительная активность их атомов и растет окислительная активность ионов.
Сравнение электродных потенциалов полуреакций позволяет сделать вывод о направлении окислительно-восстановительного процесса.
Рассмотрим гетерогенную окислительно-восстановительную реакцию, протекающую при погружении цинковой пластинки в раствор сульфата меди, диссоциирующего на ионы (рис. 5.3а):
CuSO 4 ↔ Cu 2+ + SO 4 2-
Электродные потенциалы цинка и меди имеют следующие значения:
Zn 2+ + 2е ↔ Zn 0 ; E 0 = - 0,76 B
Cu 2+ + 2 e ↔ Cu 0 ; E 0 = +0,34 B
Как видно, стандартный электродный потенциал для второй системы выше, чем для первой. Следовательно, при контакте вторая система выступит в качестве окислителя, первая - в качестве восстановителя. Другими словами, вторая реакция пойдет слева направо, а первая - в противоположном направлении, то естъ цинк будет отдавать электроны ионам меди, вытесняя, таким образом, медь из раствора ее соли (рис. 5.3 а):

Электродный потенциал возникает не только в результате обмена ионами между металлом и раствором его соли. Любая окислительно-восстановительная полуреакция характеризуется определенным значением электродного потенциала, например:
СО 2 + 4Н + + 4е ↔ С + 2Н 2 О; Е° = +0,21 B ,
NO 3 - + 4Н + + 3 e ↔ NO + 2 H 2 ; E ° = +0,96 B
В этом случае окислительные свойства сильнее выражены у иона NO 3 - , поэтому этот ион будет окислять углерод, восстанавливаясь до оксида азота NO (см.5.1).
Величина электродного потенциала не является постоянной, она зависит от ряда факторов, в частности от соотношения окисленной и восстановленной форм вещества. Эта зависимость выражается уравнением Нернста, которое при стандартной температуре 293К записывается в виде:
(5.1),
где: Е - электродный потенциал при данных концентрациях окисленной С ок и восстановленной С восст форм вещества, моль/л,
Е° - стандартный электродный потенциал,
n - число переданных электронов.
Для металлических электродов в растворах солей восстановленной формой являются атомы металла, концентрация которых - величина постоянная С M = const . В этом случае уравнение Нернста приобретает вид:
(5.2)
где:
С м + n - концентрация ионов металла, моль/л;
n - заряд иона.
Химические источники электрического тока. В рассмотренных системах переход электронов от восстановителя к окислителю осуществляется хаотически, в результате химическая энергия превращается в тепловую.
Можно, однако, пространственно разделив процессы окисления и восстановления, получить направленное движение электронов - электрический ток. Устройство, в котором химическая энергия окислительно-восстановительной реакции превращается в электрическую, называется химическим источником тока или гальваническим элементом.
Рисунок 5.3. Гетерогенный окислительно-восстановительный процесс:
а – пространственно неразделенный; в – пространственно разделенный
На рис.5.3 изображена схема гальванического элемента Даниэля - Якоби, состоящего из цинкового и медного электродов, помещенных в водные растворы сульфатов этих металлов. Растворы соединены электролитическим мостиком - трубкой, заполненной раствором электролита, например, хлорида калия. При замыкании электродов через нагрузку на цинковом электроде идет процесс окисления с выходом ионов Zn 2+ раствор; освободившиеся электроны переходят по внешней цепи на медный электрод, где восстанавливают ионы С u +2 поступающие из раствора сульфата меди.
Электрод, на котором идет процесс окисления, называется анодом, электрод, на котором протекает процесс восстановления, - катодом. В медно-цинковом элементе цинковый электрод является анодом, медный - катодом. В процессе работы элемента цинковый анод постепенно растворяется, на медном катоде осаждается медь. Таким образом, цинковый электрод является активным, его материал принимает непосредственное участие в окислительно-восстановительном процессе. Медный электрод играет пассивную роль проводника электронов, его материал в окислительно-восстановительном процессе не участвует.
Окислительно-восстановительный процесс, протекающий на электродах, нарушает ионное равновесие в растворах - у медного электрода образуется избыток ионов SO 4 2- , у цинкового - их недостаток. В результате во внутренней цепи возникает движение ионов SO 4 2- из раствора сульфата меди в раствор сульфата цинка.
Электрохимическая схема этого элемента может быть записана в виде:
где одна вертикальная черта означает границу между электронным и ионным проводниками, а две - границу между двумя ионными проводниками.
Электродвижущая сила (ЭДС) элемента при стандартных концентрациях ионов (1 моль/л) может быть вычислена как разность стандартных потенциалов катода и анода:
ЭДС = D Е° = Е 0 кат - Е 0 ан = Е 0 С u 2 +/ С u - Е 0 Zn 2 +/ Zn = +0,34 - (- 0,76) = 1,1 B .
Если концентрации ионов отличаются от стандартных, необходимо по формуле 5.2 вычислить потенциалы электродов при заданных концентрациях и затем взять их разность.
В принципе любая окислительно-восстановительная реакция может быть использована для получения электрической энергии при условии пространственного разделения процессов окисления и восстановления. Активными материалами электродов могут быть не только металлы, но и неметаллы, а также оксиды, гидроксиды и другие сложные вещества. Так, в случае реакции окисления углерода азотной кислотой (см. 5.1) электрический ток может быть получен, если в раствор азотной кислоты погрузить угольный и платиновый электроды и замкнуть их металлическим проводником. При этом активный угольный анод окисляется с образованием диоксида углерода С O 2 ,на пассивном платиновом катоде идет восстановление нитрат-ионов NO 3 - до оксида азота NO . Схема элемента может быть записана в виде:
ЭДС = D Е ° = Е ° кат - Е ° ан = Е °NO 3 - / NO - E°CO 2 / C = 0,96 - 0,21 = 0,75 В
Величина D Е° связана со стандартной энергией Гиббса реакции (D G °) соотношением:
D G °=- nF D E ° (5.3)
где n - число переданных в ходе реакции электронов, F - число Фарадея (96500Кл).
Уравнение 5.3 устанавливает связь между химической и электрической формами энергии. Оно позволяет по известному значению G рассчитать Е гальванического элемента и наоборот, зная Е рассчитать G .
Топливные элементы. Топливный элемент является разновидностью гальванического элемента, в котором электрическая энергия получается в результате окислительно-восстановительного процесса между компонентами топлива - горючим (восстановителем) и окислителем, непрерывно подводимыми к электродам извне. Горючим может служить водород, моноксид углерода, метан, спирты, а окислителем - кислород, воздух, пероксид водорода и другие вещества. Таким образом, в топливных элементах, в отличие от тепловых машин, химическая энергия топлива непосредственно превращается в электрическую, поэтому их КПД в 1,5 - 2,0 выше, чем у тепловых машин. Кроме того, они существенно меньше загрязняют окружающую среду.
Рисунок 5.4. Водородно-кислородный топливный элемент
В настоящее время практическое применение нашел водородно-кислородный топливный элемент (рис.5.4).
Он содержит два пористых металлических или угольных электрода с добавками катализатора. В качестве электролита используется водный 40 - 85% раствор гидроксида калия. Электрохимическая схема элемента:
![]()
Подаваемые к электродам газообразные водород и кислород диффундируют через электроды в направлении электролита, адсорбируются на поверхности пор и активируются катализатором. Это облегчает и ускоряет процессы окисления водорода на аноде и восстановление кислорода на катоде:
H 2 + 2 OH - - 2е ® 2 H 2 O
1/2О 2 + Н 2 О + 2е ® 2ОН -
Суммарное уравнение реакции:
Н 2 +1/2О 2 ® Н 2 О
Продукт реакции - парообразная вода отводится потоком водорода, который после отделения воды возвращается обратно в систему. Таким образом, осуществляется «холодное сжигание» водорода в кислороде с выделением энергии в электрической форме.
Аккумуляторы. Окислительно-восстановительные процессы, протекающие при работе гальванических элементов, могут иметь либо необратимый, либо обратимый характер. Соответственно химические источники тока могут быть однократного и многократного действия. Гальванические элементы многократного действия называются аккумуляторами. При работе аккумулятора в режиме источника тока самопроизвольно протекает окислительно-восстановительный процесс, приводящий к превращению химической энергии в электрическую (энергия Гиббса реакции отрицательна D G <0). Химический состав электродов при этом меняется, аккумулятор разряжается. Обратная реакция самопроизвольно не идет (D G >0). Однако разряженный аккумулятор можно зарядить от внешнего источника тока, напряжение которого превышает ЭДС элемента. При этом идет обратный процесс превращения электрической энергии в химическую и материал электродов регенерируется.
Окислительно-восстановительный процесс, протекающий при пропускании тока через электролит, называется электролизом.
В результате электролиза аккумулятор может вновь работать как источник тока. Число циклов заряд - разряд может достигать несколько сотен. В авиации находят применение свинцовый, серебряно-цинковый и кадмий-никелевый аккумуляторы.
Свинцовый (кислотный) аккумулятор в заряженном состоянии отвечает электрохимической схеме:
![]()
В режиме источника тока при разряде на отрицательном электроде происходит окисление свинца, а на положительном - восстановление диоксида свинца. При заряде идут обратные процессы: на отрицательном электроде - восстановление сульфата свинца, на положительном - его окисление:
В заряженном свинцовом аккумуляторе, в зависимости от его типа, концентрация серной кислоты составляет 27 - 30% масс. При разряде она cнижается, так как в электролит выделяется вода. Плотность электролита при этом также уменьшается. Это дает возможность, измеряя плотность электролита, контролировать степень разряда аккумулятора.
Кадмий-никелевый аккумулятор выполнен по схеме:
При разряде на отрицательном электроде Cd окисляется, на положительном - Ni (OH ) 3 частично восстанавливается. При заряде идут обратные процессы:
Кадмий-никелевые аккумуляторы стабильны в работе, требуют меньше ухода и отличаются большим сроком службы, чем свинцовые.
Серебряно-цинковый аккумулятор в заряженном состоянии соответствует схеме:
При его работе протекают обратимые реакции: на отрицательном электроде - окисление цинка, на положительном - восстановление оксида серебра:
Главным преимуществом серебряно-цинкового аккумулятора является его высокая энергоемкость; на единицу массы он дает в 4 - 6 раз больше энергии, чем рассмотренные типы аккумуляторов.
Коррозия металлов. Коррозия – это разрушение металла в результате его физико-химического взаимодействия с окружающей средой. Наиболее опасным и наиболее распространенным видом коррозии металлов является электрохимическая коррозия, которая происходит при контакте металлов с растворами электролитов. Чаще всего она является следствием работы короткозамкнутых гальванических элементов, которые образуются, например, при контакте деталей из разнородных металлов.
Роль электролита в этом случае может выполнять тонкая пленка влаги, образующаяся при адсорбции на металлических поверхностях водяного пара из атмосферы. Так, при контакте деталей из меди и железа в присутствии воды образуется гальванический элемент (рис.5.5):
Рисунок 5.5. Схема электрохимической коррозии
Железо, как более активный металл, служит анодом и подвергается окислению, на медном же катоде восстанавливается с участие воды кислород воздуха:
Для защиты металлов от коррозии используют различные покрытия: металлические, неметаллические, лакокрасочные, полимерные.
Примерные вопросы для самооценки:
1. Какие реакции называют окислительно-восстановительными?
2. Что понимают под восстановителем, окислителем?
3. В чем смысл метода электронных уравнений?
4. В чем смысл метода электронно-ионных уравнений?
5. Какие процессы называют электрохимическими?
6. Что такое стандартный водородный электрод?
7. Что является мерой окислительно-восстановительной активности системы?
8. Какую зависимость выражает уравнение Нерста?
9. Что называется гальваническим элементом?
10. Что называется катодом, анодом?
11. Как протекают окислительно-восстановительные процессы в аккумуляторах?
12. Что такое электролиз?
13. Что такое электрохимическая коррозия?
Задачи к теме № 5
Задача № 5.1.
Методом электронного баланса составить уравнения окислительно-восстановительных реакций. Указать окислитель и восстановитель:
1. NH 3 +O 2 NO+H 2 O
2. HClO 3 ClO 2 + HClO 4 +H 2 O
3. AgNO 3 Ag+NO 2 +O 2
4. NH 4 NO 2 +H 2 O
5. H 2 O 2 +PbS PbSO 4 +H 2 O
6. (NH 4) 2 Cr 2 O 7 N 2 +Cr 2 O 3 +H 2 O
7. Ca 3 (PO 4) 2 +C+SiO 2 CaSiO 3 +P+CO
8. FeS +O 2 Fe 2 O 3 +SO 2
9. N 2 H 2 +O 2 N 2 +H 2 O
10. S+KOH K 2 SO 3 +K 2 S+H 2 O
Задача № 5.2.
Составить уравнения окислительно-восстановительных реакций:
1) методом электронного баланса;
2) ионно-электронным методом.
Указать окислитель и восстановитель.
1. P+NO 3 H 3 PO 4 +NO 2 +H 2 O
2. Zn+HNO 3 Zn(NO 3) 2 NO 2 +H 2 O
3. K 2 Cr 2 O 7 +H 2 S+H 2 SO 4 S+Cr 2 (SO 4) 3 +K 2 SO 4 +H 2 O
4. KMnO 4 +KNO 2 +H 2 O KNO 3 +MnO 2 +KOH
5. FeSO 4 +H 2 O 2 +H 2 SO 4 Fe 2 (SO 4) 3 +H 2 O
6. CrCl 3 +H 2 O 2 +NaOH Na 2 CrO 4 +NaCl+H 2 O
7. CrO 3 +KNO 3 +KOH K 2 CrO 4 +KNO 2 +H 2 O
8. PH 3 +KMnO 4 +H 2 SO 4 H 3 PO 4 +K 2 SO 4 +MnSO 4 +H 2 O
9. Si+NaOH+H 2 O Na 2 SiO 3 +H 2
10. HCl+KMnO 4 Ci 2 +MnCl 2 +KCl+H 2 O
Задача № 5.3.
Решение:
Электродный потенциал рассчитывается по формуле Нернста, которая для металлических и водородного электродов записывается в виде:
где Е – электродный потенциал,
n – заряд иона металла (водорода).
Уравнение диссоциации сульфата железа:
Fe 2 SO 4 2 Fe 3+ +3 SO 4 2-
показывает, что при диссоциации 0,05 моль Fe 2 (SO 4) 3 образуется 0,05 2=0,1 моль ионов Fe 3+ .
Следовательно С(Fe 3+ )=0,1 моль/л, n =3.
Из таблицы 3 имеем E 0 (Fe3+/Fe)=-0,04.
Задача № 5.4.
Задача № 5.5.
На сколько изменится потенциал цинкового электрода, если раствор соли цинка, в который он погружен разбавить в 10 раз.
Задача № 5.6.
Потенциал кадмиевого электрода в растворе его соли равен 0,52В. Рассчитать концентрацию ионов Сd + в растворе.
Задача № 5.7.
Задача № 5.8.
Вычислить рН раствора, в котором потенциал водородного электрода равен – 100 mB.
Задача № 5.9.
|
Уравнение реакции |
Концентрация ионов, С моль/л |
рН |
MnO 4 - +8H + +5 e Mn 2+ +4H 2 O |
C(MnO4-)=C(Mn2+)=1 |
ClO 3 - +6H + +6e Cl - +3H 2 O |
C(ClO 3 -)=C(Cl -)=0,1 |
Cr 2 O 7 2- +14H + +6e 2Cr 3 ++7H 2 O |
C(Cr 2 O 7 2-)=C(Cr 3+)=1 |
PbO 2+ 4H + +2e Pb 2 ++2H 2 O |
C(Pb 2+)=0,1 |
Решение 1:
Потенциал окислительно-восстановительного электрода Е рассчитывают по уравнению Нерста:
где Е 0 стандартный электродный потенциал;
n – число участвующих в реакции электронов;
С ок, С восст – произведения концентраций веществ, находящихся в окисленной и восстановленной формах соответственно.
В данной системе в окисленной форме находятся ионы Mn 4 - и H + , в восстановленной – ион Mn 2+ и молекула Н 2 О. В реакции принимает участие 5 электронов. Учитывая, что концентрация воды практически остается постоянной и входит в значение Е 0 , имеем:
По данным таблицы 3: Е 0 (MnO 4 - /Mn 2+)=+1,51В.
Подставляя числовые значения получим окончательно:
Задача № 5.10.
Написать уравнения электродных процессов, протекающих при работе гальванического элекмента. Вычислить ЭДС элемента при заданных концентрациях, С моль/л.
|
Схема элемента |
С, моль/л |
Zn/Zn 2+ //Pb 2+ /Pb |
C(Zn2 +)=0,2, C(Pb 2+)=0,04 |
Mn/Mn 2+ //Ni 2+ /Ni |
C(Mn 2+)=0,1, C(Ni 2+)=0,01 |
Fe/Fe 2+ //Cu 2+ /Cu |
C(Fe 2+)=1, C(Cu 2+)=0,5 |
H 2 /2H + //Ag + /Ag |
C(H +)=0,01, C(Ag +)=0,1 |
Ni/Ni 2+ (C 1)//Ni 2+ (C 2)/Ni |
C 1 (Ni 2+)=0,1, C 2 (Ni 2+)=0,01 |
Cu/Cu 2+ //Fe 3+ /Fe 2+ |
C(Cu 2+)=1, C(Fe 3+)=C(Fe 2+)=1 |
Решение 1:
На основании данных таблицы 3 можно заключить, что более активный металл цинк будет в данном элементе анодом, а менее активный металл свинец – катодом.
ЭДС гальванического элемента равна разности электродных потенциалов окислителя (катода) и восстановителя (анода):
Используя формулу Нерста, имеем:
Задача № 5.11.
Установить, в каком направлении возможно самопроизвольное протекание в стандартных условиях данной реакции. Рассчитайте величину константы равновесия реакции.
|
Уравнение реакции |
2С l - + 2Fe 3+ 2Fe 2+ +Cl 2 |
H 2 O 2 +HClO H + Cl+O 2 +H 2 O |
5H 2 O 2 +H + +2IO 3 I 2 +5O 2 +6H 2 O |
Sn 4+ +2I - Sn 2+ +I 2 |
Sn 4+ +H 2 S Sn 2+ +S+2H + |
H 2 S+4H 2 O 2 2H + +SO4 2- +4H 2 O |
Решение 1:
Для определения направления окислительно-восстановительной реакциинеобходимо найти ЭДС гальванического элемента, образованного из дпнного окислителя и восстановителя.
где Е 0 ок, Е 0 восст – стандартные потенциалы окислителя и восстановителя.
Возможна та реакция, для которой, так как в этом случае изменение энергии Гиббса – отрицательная величина.
где n - число участвующих в реакции электронов;
F – число Фарадея, равное 96480 Кл/моль.
В свою очередь, изменение энергии Гиббса связано с константой равновесия соотношением:
Следовательно,
откуда
, .
Стандартные электродные потенциалы равны (см. таблицу 3):
Cl 2 + 2e 2Cl - E 0 (Cl 2 /2Cl -)=1,36 B
Fe 3+ + e Fe 2+ E 0 (Fe 3+ /Fe 2+ =0,77 B
Поскольку Е 0 (С l 2 /2С l )> E 0 (Fe 3+ / Fe 2+ ) окислителем будет служить хлор, а восстановителем – ион Fe 2+ .
Уравнения электродных процессов:
Суммарное уравнение:
Cl 2+ 2Fe 2+ 2 Cl - + Fe 3+
Таким образом, рассматриваемая реакция будет протекать справа налево.
К=10 20
Задача №5.12.
Рассчитать величину потенциала окислительно-восстановительного электрода, полученного при погружении платиновой проволоки в водный раствор, содержащий одновременно две соли А и В с концентрациями С А и С В, моль/л при заданном значении водородного показателя рН.
|
С А |
С В |
рН |
Na 2 Cr 2 O 7 |
Cr 2 (SO 4) 3 |
0,2 |
4 |
2 |
NaClO 2 |
NaClO |
0,1 |
0,3 |
9 |
3 |
KClO 4 |
NaClO3 |
0,2 |
0,3 |
3 |
4 |
Na 2 SO 4 |
K 2 SO 3 |
0,05 |
0,08 |
10 |
5 |
CrCl 3 |
CrCl 2 |
0,2 |
0,8 |
1 |
6 |
NaNO 3 |
NaNO 2 |
0,01 |
0,09 |
9 |
7 |
Na 2 S 2 O 8 |
Na 2 SO 4 |
0,1 |
0,2 |
6 |
8 |
KMnO 4 |
K2MnO 4 |
0,3 |
0,6 |
8 |
9 |
Fe 2 (SO 4) 3 |
FeSO 4 |
1 |
3 |
2 |
10 |
Ce(SO 4) 2 |
Ce 2 (SO 4) 3 |
0,002 |
0,001 |
0,5 |
Решение 1:
Раствор, содержащий одновременно окисленную и восстановленную форму одного и того же элемента (в данном случае, хрома), называется окислительно-восстановительной системой. В общем виде уравнение окислительно-восстановительной реакции для окислительно-восстановительного электрода имеет вид:
Ох+ ne Red ,
где n – число электронов, участвующих в реакции, а Ох и Red – окисленная и восстановленная форма элемента. Для определения величины электродного потенциала такой системы следует воспользоваться уравнением Нерста:
Формально в данном случае степень окисления в электродном процессе изменяет хром
Cr 6+ + 3 e Cr 3+ ,
то есть окисленной формой будет Cr 6+ - содержащая форма, однако это не означает, что можно записать по логарифмом в уравнении Нерста величину активности Cr 6+ . Это связано с тем, что сама по себе частица С r 6+ в водном растворе не существует, она входит в состав более сложной частицы Cr 2 O 7 2- , поэтому понятие активности, то есть кажущейся концентрации несуществующих частиц Cr 6+ лишено смысла. Можно определить активность (или концентрацию) частиц Cr 2 O 7 2- , но тогда и уравнение электродного процесса следует записать с участием частиц Cr 2 O 7 2-
Cr 2 O 7 2- +…. Cr 3+ +…,
однако в этом случае в левой части присутствует кислород, а в правой его нет, поэтому необходимо дописать в правую часть частицы, содержащие О 2- . Ионов О 2- в водном растворе нет, однако кислород с такой степенью окисления входит в состав либо молекул Н 2 О, либо ионов ОН - . Поскольку по условию среда является кислой (рН<7), концентрация ионов ОН - в этом растворе крайне мала, значит следует записывать электродный процесс на с участием этих ионов, а с участием молекул Н 2 О
Cr 2 O 7 2- + 14Н+ + 6е 2С r 3+ + 7 H 2 O
Таким образом, в электродном процессе помимо ионов Cr 2 O 7 2- и С r 3+ участвуют и ионы Н + , поэтому их концентрация также будет влиять на величину электродного потенциала, то есть
По условию, концентрации К 2 Cr 2 O 7 и Cr 2 (SO 4 ) 3 составляют соответственно 0,1 и 0,2 моль/л. Поскольку эти соли являются сильными электролитами, то есть диссоциируют в растворе нацело, концентрация ионов Cr 2 O 7 2- и Cr 3+ составят 0,1 и 0,4 моль/л. При рН=2 концентрация ионов Н + равна С(Н +)=10 -рН =10 -2 , отсюда:
Ключевые понятия:
· реакция окисления;
· реакция восстановления;
· окислитель;
· восстановитель;
· уравнение окислительно-восстановительной реакции;
· электрохимическая система;
· стандартный водородный электрод;
· стандартный электродный потенциал;
· химический источник тока;
· катод;
· анод;
· топливный элемент;
· аккумулятор;
· электролиз;
· коррозия.
381. Степенью окисления элемента называют:
382. Как называется валентность атома со знаком его электровалентности:
383. Чему равна алгебраическая сумма степеней окисления всех атомов, входящих в состав молекулы:
384. Реакции, в результате которых изменяются степени окисления элементов, называются:
385. Окислитель и восстановитель:
386. Количество окислителя, которое присоединяет 1 моль электронов в данной окислительно-восстановительной реакции, называется:
387. Какая реакция является окислительно-восстановительной:
388. Чему равна степень окисления хлора в перхлорате калия (КСlО 4):
389. Чему равна степень окисления атома хрома в молекуле Сr 2 (SО 4) 3:
390. Чему равна степень окисления Mn в соединении КМnО 4:
391. Чему равна степень окисления атома хрома в молекуле К 2 Сr 2 О 7:
392. Определите степень окисления Mn в соединении К 2 MnО 4:
393. Какая из окислительно-восстановительных реакций является реакцией диспропорционирования:
394. Какая из окислительно-восстановительных реакций является внутримолекулярной:
395. Процесс ClO 3 - ® Cl - представляет собой:
396. Укажите конечный продукт превращения иона MnO в щелочной среде:
397. Укажите конечный продукт превращения иона MnO в кислой среде:
398. Укажите конечный продукт превращения иона MnO в нейтральной среде:
399. Чему равно число электронов, участвующих в полуреакции окисления сульфит-иона SO до сульфат-иона SО :
400. Чему равно число электронов, участвующих в полуреакции окисления сульфид-иона S 2- до сульфат-иона SО :
401. Чему равно число электронов, участвующих в полуреакции восстановления сульфит-иона SO до сульфид-иона S 2- :
402. Чему равно число электронов, участвующих в полуреакции восстановления иона MnO до иона Mn 2+ :
403. Чему равно число электронов, участвующих в полуреакции окисления иона S 2- до иона SО :
404. Коэффициент перед формулой окислителя в уравнении реакции между алюминием и бромом равен:
405. Коэффициент перед формулой восстановителя в уравнении реакции между алюминием и бромом равен:
406. Коэффициенты перед формулами восстановителя и окислителя в уравнении реакции, схема которой Р + КСlО 3 = КСl + Р 2 О 5:
407. Коэффициент перед формулой восстановителя в уравнении реакции, схема которой Mg + HNO 3 = N 2 O + Mg(NO 3) 2 + H 2 O:
408. В уравнении реакции, схема которой Р + НNО 3 + Н 2 О =Н 3 РО 4 + NО, коэффициент перед формулой восстановителя равен:
409. Чему равен эквивалент восстановителя в окислительно-восстановительной реакции: 2Н 2 S + Н 2 SО 3 = 3S + 3Н 2 О:
410. Чему равна эквивалентная масса восстановителя в реакции HNO 3 + Ag = NO + AgNO 3 + H 2 O:
411. Укажите эквивалент окислителя реакции HNO 3 + Ag = NO 2 + AgNO 3 + H 2 O:
412. При взаимодействии концентрированной азотной кислоты с металлическим натрием образуются продукты:
413. До какого вещества идет восстановление концентрированной азотной кислоты при ее взаимодействии с серебром:
414. С неметаллами разбавленная азотная кислота восстанавливается до образования:
415. Укажите продукты взаимодействия разбавленной азотной кислоты с фосфором:
416. Продуктами взаимодействия разбавленной серной кислоты с медью, являются:
417. Какие металлы вытесняют водород в реакции их взаимодействия с разбавленной серной кислотой:
Электрохимия
418. Что изучает электрохимия:
419. Что является основой электрохимических явлений:
420. Составляющие простейшей электрохимической системы:
421. Проводниками 1-го рода в электрохимической системе являются:
422. Проводниками 2-го рода в электрохимической системе могут выступать:
423. Внешней цепью электрохимической системы являются:
424. Счетчики количества электричества (кулонометры, интеграторы тока) и другие устройства, созданы на основе законов:
425. Формулировка: «Количество вещества, образовавшегося на электроде при электролизе, прямо пропорционально количеству прошедшего через электролит тока», является отражением:
426. Согласно закону Фарадея, какое количество электричества необходимо затратить для выделения одного грамм-эквивалент любого вещества при электролизе:
427. Процессы окисления в электрохимии получили название:
428. Катодными процессами в электрохимии называются:
429. Электроды, на которых осуществляются процессы окисления:
430. Электроды, на которых осуществляются процессы восстановления:
431. Суммарная химическая реакция, протекающая в гальваническом элементе, называется:
432. Как обозначают границу раздела между проводником первого и второго рода при схематической записи гальванического элемента:
433. Как обозначают границу раздела между проводниками второго рода при схематической записи гальванического элемента:
434. Максимальная разность потенциалов электродов, которая может быть получена при работе гальванического элемента:
435. Максимальное значение напряжения гальванического элемента, соответствующее обратимому протеканию реакции, называется:
436. Стандартным электродным потенциалом (φ°), называют:
437. Если из ряда стандартных электродных потенциалов выделить процессы Ме z + + Zе = Ме, то получим значения, образующие:
438. Формула Нернста, отражающая зависимость электродного потенциала металла от различных факторов имеет следующее математическое отражение:
439. Изменение потенциала электрода при прохождении тока:
440. Что изучает электрохимическая кинетика:
441. Устройство однократного применения, преобразующее энергию химических реакций в электрическую энергию:
442. Составляющими простейшего гальванического элемента являются:
443. Ток силой 2,5 А проходя через раствор электролита, за 30 мин выделяет из раствора 2,77 г металла. Чему равна эквивалентная масса металла:
444. Ток силой 6 А пропускали через водный раствор серной кислоты в течении 1,5 ч. Чему равна масса разложившейся воды (г):
445. Ток силой 6 А пропускали через водный раствор серной кислоты в течении 1,5 ч. Чему равен объем (л) выделившегося водорода (условия нормальные):
446. Ток силой 6 А пропускали через водный раствор серной кислоты в течении 1,5 ч. Чему равен объем (л) выделившегося кислорода (условия нормальные):
447. При работе какого гальванического элемента проходят процессы Zn -2e = Zn 2+ ; Cu 2+ + 2e = Cu:
448. Укажите схему железо-медного гальванического элемента:
449. Схема цинк-магниевого гальванического элемента:
450. Укажите схему никель-медного гальванического элемента:
451. Химическая реакция, лежащая в основе анодного процесса, при заряде кислотного аккумулятора:
452. Химическая реакция, лежащая в основе катодного процесса, при заряде кислотного аккумулятора:
453. Какой процесс при работе свинцового аккумулятора отображает химическая реакция PbO 2 + 2H 2 SO 4 = PbSO 4 + SO 2 + 2H 2 O:
454. Какой процесс при работе кислотного аккумулятора отображает химическая реакция Pb + H 2 SO 4 = PbSO 4 + H 2:
455. Химическая реакция, лежащая в основе катодного процесса, при заряде кислотного аккумулятора:
456. Химическая реакция, лежащая в основе анодного процесса, при заряде кислотного аккумулятора:
457. В щелочных аккумуляторах ионным проводником служит 20%-ный раствор:
458. Общее название аккумулятора в котором токообразующей реакцией служит 2NiOOH + Cd + 2H 2 O →2Ni(OH) 2 + Cd(OH) 2:
459. Положительный электрод в щелочных аккумуляторах содержит:
460. Отрицательные пластины в щелочном аккумуляторе, где протекает токообразующая реакция Ni OOH+Fe + 2H 2 O →2Ni(OH) 2 + Fe(OH) 2
461. На обоих электродах при разрядке кислотного аккумулятора образуется:
462. Из какого металла состоят положительные пластины кадмиево-никелевых щелочных аккумуляторов:
463. Отрицательные платины кадмиево-никелевых щелочных аккумуляторов состоят:
464. Положительные пластины серебряно-цинкового щелочного аккумулятора изготавливают из:
465. Из какого металла изготовлены отрицательные платины серебряно-цинкового щелочного аккумулятора:
466. В каких случаях в электролизер вводится пористая перегородка – диафрагма:
467. Что является материалом для изготовления диафрагмы при работе электролизера:
468. Какой процесс происходит на катоде при электролизе раствора сульфата калия K 2 SO 4:
469. Какой процесс происходит на инертном аноде при электролизе сульфата натрия Na 2 SО 4:
470. Укажите соль, при электролизе которой на аноде выделяется свободный кислород:
471. Ионное уравнение катодного процесса 2Н 2 О + 2е = Н 2 + 2ОН - возможно при электролизе соли:
472. Ионное уравнение анодного процесса 2Н 2 О - 4е = О 2 + 4Н + возможно при электролизе соли:
473. Никелевые пластинки опущены в водные растворы перечисленных ниже солей. С какими солями никель будет реагировать?
474. Цинковые пластинки опущены в водные растворы перечисленных ниже солей. С какой солью цинк будет реагировать:
475. Укажите свойство железа, которое отрицательно влияет на его использование в технике:
476. В голубой раствор хлорида меди (II) опускают очищенный железный гвоздь, который быстро покрывается налетом меди. Раствор при этом приобретает зеленоватое окрашивание, объясняющееся:
477. Лампочка прибора для испытания веществ на электрическую проводимость загорится при погружении электродов в:
478. Как будет изменяться свечение лампочки в приборе для испытания электропроводности растворов, если его электроды опустить в известковую воду, через которую пропускать оксид углерода (IV)? Почему?
479. Укажите металл, характеризующийся полной термодинамической стабильностью к электрохимической коррозии:
480. До недавнего времени консервные банки изготавливали из так называемой белой жести (железного корпуса, покрытого защитным слоем олова). В открытых консервных банках не рекомендуется сохранять продукты, так как, если поцарапан защитный слой, банка быстро ржавеет. Укажите реакции, лежащие в основе данного процесса.
481. Электронное уравнение анодного процесса атмосферной коррозии луженого железа:
482. Электронное уравнение катодного процесса атмосферной коррозии луженого железа:
Полимеры
483. Процесс образования полимеров из низкомолекулярных веществ, сопровождающийся выделением побочного продукта (воды, аммиака, хлороводорода и др.).
|
Аккумулятор |
Удельная энергия, |
Удельная мощность, |
Срок службы, число циклов |
|
|
Pb-кислотный | ||||
|
Fe-воздушный | ||||
|
Zn-воздушный | ||||
|
Zn-хлоридный | ||||
|
Na-сульфидный | ||||
|
Li-сульфидный |
Свинцовый аккумулятор
Самое большое распространение пока получил свинцово-кислотный аккумулятор. Он служит источником тока для стартеров двигателей внутреннего сгорания, для аварийного освещения, радио- и телефонной аппаратуры, используется на подводных аппаратах и станциях и других целей.
Pb-кислотный аккумулятор состоит из свинцового анода и катода в виде свинцовой решетки, набитой оксидом свинца (IV). Электролитом служит серная кислота. При работе ЭА на одном электроде (аноде) протекают реакции, при которых степень окисления свинца меняется от 0 до +2 (разряд) и от +2 до 0 (заряд), а на другом электроде (катоде) степень окисления свинца меняется от +4 до +2 (разряд) и наоборот (заряд).
|
На аноде: | |
|
На катоде: | |
|
Суммарная токообразующая реакция описывается уравнением: |
Ток, получаемый от свинцового аккумулятора, может быть усилен, если сконструировать катод в виде ряда пластин, которые чередуются с несколькими анодными пластинами (рис.9.4). Каждый такой ЭА дает напряжение, приблизительно равное 2 В. Батареи, используемые в автомобилях, обычно состоят из шести таких аккумуляторов, соединенных последовательно и дающих напряжение около 12 В.
Электролиз.
В
растворах и расплавах электролитов
имеются разноименные по знаку ионы
(катионы и анионы), которые подобно всем
частицам жидкости находятся в хаотическом
движении. Если в такой расплав электролита,
например расплав NaCl
(![]() )
погрузить электроды и пропустить
постоянный электрический ток, то ионы
будут двигаться к электродам: катионы
)
погрузить электроды и пропустить
постоянный электрический ток, то ионы
будут двигаться к электродам: катионы
Na + +=Na 0
(катод)
2Cl - - 2e=Cl 2 (анод)
Эта реакция является ОВР на аноде протекает процесс окисления, на катоде- процесс восстановления.
Электролиз – это окислительно - восстановительный процесс, протекающий на электродах при прохождении электрического тока через раствор или расплав электролита.
Суть электролиза состоит в осуществлении за счет электрической энергии химических реакций – восстановления на катоде и окисления на аноде. При этом катод отдает электроны катионам, а анод принимает электроны от анионов.
Процесс электролиза наглядно изображают схемой, которая показывает диссоциацию электролита, направления движения ионов, процессы их электродах и выделяющихся веществ. Схема электролиза NaCl:
Катод Анод
Для проведения электролиза электроды погружают в раствор или расплав электролита и соединят их с источником тока. Прибор, на котором проводят электролиз называют электролизером или электролитической ванной.
Электролиз водных растворов электролитов.
При электролизе растворов электролитов в процессах могут участвовать молекулы воды. Для восстановления к катоду надо приложить потенциал равныйВ, а для восстановления молекул водыВ.
Поэтому на катоде будут восстанавливаться катионы воды:
катод
![]()
а на аноде будут окисляться хлорид ионы:
Ионы накапливаются около катода и совместно с ионамиобразуют гидроксид натрия.
Катодные и анодные процессы
Катионы металлов, имеющих стандартный потенциал больший, чем у
водорода (от довключительно), при электролизе плотность восстанавливаются на катоде.
Катионы металлов, имеющих малую величину стандартного
электродного потенциала (от довключительно), не восстанавливаются на катоде, а вместо них восстанавливаются молекулы воды.
Если же водный раствор содержит катионы различных металлов, то при электролизе выделяющие их на катоде протекают в порядке уменьшения стандартного электродного потенциала соответствующего металла.
сначала .
Характер реакций протекающих на аноде зависит от присутствия молекул так и от вещества, из которого сделан анод. обычно аноды подразделяются на растворимые(Cu, Ag, Zn, Cd, Ni) и нерастворимые(уголь, графит, Pt,).
На растворимом аноде в процессе электролиза происходит окисление анионов (если кислоты безкислородные –) если же раствор содержит анионы кислородосодержащих кислот () то на аноде окисляются не эти ионы, а молекулы воды:
Растворимы анод при электролизе окисляется, т.е. посылает во внешнюю цепь.
и анод растворяется.
Как протекает электролиз с нерастворимым (угольными) электродами?
Пример 2. с нерастворимым электродом.
Катод Анод
![]() e
e

если
катодное и анодное пространство не
разделены перегородкой, то:
Пример 4. Электролиз раствора
Электроды из меди
Катод (Cu) Анод: e
5) Электролиз c электродами
Закон Фарадея
Это количественный закон электролиза
m- масса вещества. которые выделяются на электродах (г)
n- число электронов, которыми обмениваются окислитель и восстановитель
I - сила тока (А)
М- молярная масса вещества, которая выделяется на электроде
F- постоянная Фарадея 96485
t- время (сек)
Причиной возникновения и протекания электрического тока в гальваническом элементе является разность электродных потенциалов.
Стандартный потенциал восстановления - количественная мера способности вещества (молекулы или иона) вступать в окислительно-восстановительные реакции в водном растворе.
Окислительно-восстановительная реакция возможна, если
![]() где
где
- стандартный потенциал восстановления окислителя.
Стандартный потенциал восстановления восстановителя.
Уравнение Нернста:

где - электродный потенциал металла, В;
Стандартный электродный потенциал металла, В;
Универсальная газовая постоянная (8,31 Дж/моль;
Абсолютная температура, К;
Число электронов, участвующих в реакции;
Постоянная Фарадея (96 500 Кл/моль).
ЭДС любого гальванического элемента можно вычислить по разности стандартных электронных потенциалов Е о. При этом следует иметь в виду, что ЭДС всегда положительная величина. Поэтому надо из потенциала электрода, имеющего большую алгебраическую величину, вычислить потенциал, алгебраическая величина которого меньше.
Е= Е о си - Е о zn = (+ 0,34) - (-0,76) = 1,10 В
Е= Е о ок-ль - Е о вос-ль
Е о ок-ль – потенциал электрода с большей алгебраической величиной.
Е о вос-ль – потенциал электрода с меньшей алгебраической величиной.
Некоторые стандартные электродные потенциалы приведены в приложении 4.
Количественная характеристика процессов электролиза определяется законом Фарадея :
Масса электролита, подвергшегося превращению при электролизе, а также масса образующихся на электродах веществ прямо пропорциональны количеству электричества, прошедшего через раствор или расплав электролита, и эквивалентным массам соответствующих веществ.
Закон Фарадея выражается следующим уравнением:
Где - масса образовавшегося или подвергшегося превращению вещества;
Э – его эквивалентная масса, г экв;
I – сила тока, А;
t – время, сек;
F – число Фарадея (96 500 Кл/моль), т.е. количество электричества, необходимое для осуществления электрохимического превращения одного эквивалента вещества.
Пример 1 : Сколько граммов меди выделится на катоде при электролизе раствора CuSO 4 в течение 1 ч при силе тока 4 А.
Решение : Эквивалентная масса меди в CuSO 4 равна =, подставляя в уравнение Фарадея значения Э = 32,I = 4 А, t = 6060 = 3600 с, получим
![]() = 4,77 г.
= 4,77 г.
Пример 2 : Вычислите эквивалент металла, зная, что при электролизе раствора хлорида этого металла затрачено 3880 Кл электричества и на катоде выделяется 11, 74 г металла.
Решение : Из уравнения Фарадея выводим Э = , гдеm= 11,742 г; F = 96 500 Кл/моль; It = Q = 3880 Кл.
Э =
![]() =
29,35
=
29,35
Пример 3 : Сколько граммов гидроксида калия образовалось у катода при электролизе раствора K 2 SO 4 , если на аноде выделилось 11,2 л кислорода (н.у.)?
Решение : Эквивалентный объем кислорода (н.у.) 22,4/4 = 5,6 л. Следовательно, 11,2 л содержат 2 эквивалентные массы кислорода. Столько же эквивалентных масс КОН образовалось у катода. Или 56 2 = 112, 7 (56 г/моль – мольная и эквивалентная масса КОН).
Свинцово–кислотный аккумулятор – на данный момент, этот тип аккумуляторов считается наиболее распространённым, нашел широкую область применения как автомобильный аккумулятор.
Принцип действия аккумулятора
Принцип действия, как говорилось ранее в статье про аккумуляторы , основан на окислительно-восстановительной электрохимической реакции. В данном случае на реакции свинца с диоксидом свинца, находящихся в сернокислотной среде. Во время использования аккумулятора, происходит разряд – на аноде будет происходить восстановление диоксида свинца, а на катоде – окисление свинца.
Во время зарядки аккумулятора, будут проходить ровно обратные реакции, с выделением кислорода на положительном электроде, и выделением водорода на отрицательном. Следует учесть, что на критических значениях, когда происходит зарядка и аккумулятор почти заряжен, может начать преобладать реакция электролиза воды, что приведет к её постепенному исчерпанию.
В итоге, можно сказать, что при заряде серная кислота будет выделяться в электролит, что влечет за собой повышение плотности электролита, а при разряде серная кислота будет расходоваться, и плотность будет падать.
Устройство аккумулятора
Свинцово-кислотный аккумулятор состоит из электродов, разделительных сепараторов (ячеек, изоляторов), которые находятся в электролите. Сами электроды на вид – это свинцовые решетки, только с разным активным веществом, положительный электрод имеет активное вещество – диоксид свинца (PbO 2), отрицательный электрод – свинец.

Рисунок 1 – Общий вид свинцово-кислотного аккумулятора

Рисунок 2 – Ячейка аккумулятора с положительными и отрицательными электродами, разделёнными сепараторами
На рисунке 1 вы можете видеть в моноблоке отдельные ячейки подробно рассмотренные на рисунке 2 – в которых находятся положительные и отрицательные электроды, разделённые сепараторами.
Эксплуатация свинцово-кислотного аккумулятора при низких температурах
В отличии от других типов аккумуляторов, свинцово-кислотные более-менее устойчивы к холоду, как мы видим в последствии – широкое применение на автотранспорте. Свинцово-кислотный аккумулятор теряет 1% своей ёмкости на каждый градус отличный от +20°C, что говорит о том, что при 0°C ёмкость свинцово-кислотного аккумулятора будет составлять лишь 80% его ёмкости. Это обусловлено увеличением вязкости электролита при низких температурах, из-за чего он не может поступать в нормальной степени к электродам, а тот электролит что поступает, быстро истощается.
Зарядка аккумулятора
Для большинства аккумуляторов ток зарядки должен быть написан на корпусе, примерно, он может находиться в пределах от 0.1 до 0.3 емкости аккумулятора. Вообще, общепринятым считается зарядка аккумулятора 10% током от его ёмкости, на протяжении 10 часов. Максимальное напряжение при зарядке не должно превышать 2.3 ± 0.023 В на каждый из элементов аккумулятора. То есть, можно сказать что для свинцового аккумулятора с напряжением в 12 В, напряжение во время зарядки не должно превышать 13.8 ± 0.15 В.
Хранение свинцово кислотных аккумуляторов
Свинцово-кислотные аккумуляторы хранятся только в заряженном состоянии. Хранение их в разряженном состоянии приводит к потере работоспособности.
Электрохимия
Зайлобов Л. Т., аспирант Ташкентского государственного педагогического университета им. Низами (Узбекистан)
ДЕМОНСТРАЦИЯ ПРОЦЕССОВ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ, ПРОХОДЯЩИХ В СВИНЦОВОМ АККУМУЛЯТОРЕ, С ПРИМЕНЕНИЕМ ИННОВАЦИОННЫХ ТЕХНОЛОГИЙ
Представлена анимационная модель демонстрации процессов окислительно-восстановительных реакций, проходящих в свинцовом аккумуляторе, с применением инновационных технологий. Данная статья рекомендована для учащихся академических лицеев и колледжей с углубленным изучением химии.
Ключевые слова: окислительно-восстановительные реакции, гальванические элемент, батарея, свинцовом аккумуляторе, растворе H2S04, электрод, анимационная модель, металлического свинца, исход электрического тока - разряд, восстановление - заряд, ионы, электропроводность.
DEVELOPMENT OF EDUCATION ON OXIDATION-REDUCTION REACTIONS OCCURRING IN LEAD CELLS USING INNOVATIVE TECHNOLOGIES
Is presented animation model the development of the tuition of oxidizing-reсonstruсtion reactions passing in plumbum battery with applying of innovation technologies. This article is recommended for taken into account academic lyceums and colleges with the in-depth studies of chemistry.
Keywords: oxidizing-reconstruction reactions, galvanic element, a batterie, leaden battery, solution H2S04, electrode, animation model, metallic lead, upshot of the electric current - a category, reconstruction - a charge, Ions, conduction.
В настоящее время широко используемые гальванические элементы - батареи и аккумуляторы являются неотъемлемой частью нашей жизни. Окислительные и восстановительные процессы, которые проходят в аккумуляторах, являются одной из трудноосваиваемых тем общей химии. Объяснение данной темы без наглядных пособий и химических опытов является основной причиной этой проблемы.
Периодические перемещения электронов в окислительных и восстановительных реакциях, проходящие в гальванических элементах, можно показать только при помощи инновационных технологий. Динамичная модель этих процессов демонстрируется с помощью компьютера. Готовые электронные данные и проведение компьютерных уроков на основе анимации и их демонстрация ученикам повышают качество урока.
Свинцовая аккумуляторная батарея. В элементах протекают следующие реакции: На эноде: Pb+SO43^PbSO4+24
На катоде: Pb O2+ SO42+24^ PbSO4+2H2O Батарея обладает свойством обратимости (может перезаряжаться), поскольку продукт протекающих с ней реакций - образующийся на обоих электродах сульфат свинца - оседает на пластинах, а не диффундирует и не отваливается от них. Один элемент изображенный здесь свинцовой аккумуляторной батареи дает напряжение около 2 В; в батареях на 6 или 12 В последовательно соединены три или шесть описанных элементов.
Первый работоспособный свинцово-кислотный аккумулятор был изобретен в 1859 г. французским ученым Гастоном Планте. Конструкция аккумулятора представляла собой электроды из листового свинца, разделенные сепараторами из полотна, которые были свернуты в спираль и помещены в сосуд с 10 % раствором серной кислоты. Недостатком первых свинцово-кислотных аккумуляторов была их невысокая емкость.
В качестве примера рассмотрим готовый к употреблению свинцовый аккумулятор. Он состоит из решетчатых свинцовых пластин, одни из которых заполнены диоксидом свинца, а другие - металлическим губчатым свинцом. Пластины погружены в 35-40% раствор Н2804; при этой концентрации удельная электропроводность раствора серной кислоты максимальна.
При работе аккумулятора - при его разряде - в нем протекает окислительно-восстановительная реакция, в ходе которой металлический свинец окисляется:
РЬ+804-2=РЬ804+2ё или РЬ-2ё=РЬ+2
А диоксид свинца восстанавливается:
РЬ02+2Н2804=РЬ(804)2+2Н20
РЬ(804)2+2ё= РЬ804+ 80^2 или РЬ+4+2ё=РЬ
Электроны, отдаваемые атомами металлического свинца при окислении, принимаются атомами свинца РЬ02 при восстановлении; электроны передаются от одного электрода к другому по внешней цепи.
Таким образом, были созданы и испытаны химические процессы, проходящие в аккумуляторах в виде анимационной модели. В ней показан исход электрического тока - разряд и восстановление - заряд. Появление каждой реакции объясняется движением ионов в растворе.
р-1,23-1,27 гр/мл
Во внутренней цепи (в растворе Н2804) при работе аккумулятора происходит перенос
ионов. Ионы 804 движутся к аноду, а ионы Н+ - к катоду. Направление этого движения обусловлено электрическим полем, возникающим в результате протекания электродных процессов: у анода расходуются анионы, а у катода - катионы. В итоге раствор остается электронейтральным.
Если сложить уравнения, отвечающие окислению свинца и восстановлению РЬ02, то получится суммарное уравнение реакции, протекающей в свинцовом аккумуляторе при его работе (разряде):
РЬ + РЬ02 + 4Н++ 2Б04
2РЬБ04 + 2Н2О
Э.д.с. заряженного свинцового аккумулятора равна приблизительно 2В. По мере разряда аккумулятора материалы его катода (РЬ02) и анода (РЬ) расходуются. Расходуется и серная кислота. При этом напряжение на зажимах аккумулятора падает. Когда оно становится меньше значения, допускаемого условиями эксплуатации, аккумулятор вновь заряжают.
Для зарядки (или заряда) аккумулятор подключают к внешнему источнику тока (плюсом к плюсу и минусом к минусу). При этом ток протекает через аккумулятор в направлении, обратном тому, в котором он проходил при разряде аккумулятора. В результате этого электрохимические процессы на электродах «обращаются». На свинцовом электроде теперь происходит процесс восстановления:
РЬ804+2Н++2ё = Н2Б04 + РЬ т.е. данный электрод становится катодом. На электроде из РЬ02 идет процесс окисления:
РЬ804+2Н+-2ё=РЬ02+Н2804+2Н+
Следовательно, этот электрод является теперь анодом. Ионы в растворе движутся в направлениях, обратных тем, в которых они перемещались при работе аккумулятора.
Складывая два последних уравнения, получим уравнение реакции, протекающей при зарядке аккумулятора:
2РЬБ04 + 2Ш0^РЬ + РЬ02 + 2Н2Б04
Нетрудно заметить, что этот процесс противоположен тому, который протекает при работе аккумулятора: при зарядке аккумулятора в нем вновь получаются вещества, необходимые для его работы.
Свинцовые аккумуляторы являются наиболее распространенными среди всех существующих в настоящее время химических источников тока. Их масштабное производство определяется как относительно низкой ценой, обусловленной сравнительной недефицитностью исходных материалов, так и разработкой разных вариантов этих аккумуляторов, отвечающих требованиям широкого круга потребителей.
Применение наглядной демонстрации процессов, проходящих в данном свинцовом аккумуляторе, использование анимационной модели позволяет учащимся легче усвоить столь трудную для понимания тему.
ЛИТЕРАТУРА
1. Р.Дикерсон, Г.Грей, Дж.Хейт. Основные законы химии. Издательство «Мир» Москва 1982. 653с.
2. Деордиев С.С. Аккумуляторы и уход за ними. К.: Техника, 1985. 136с.
3. Электротехнический справочник. В 3-х т. Т.2. Электротехнические изделия и устройства/под общ. ред. профессоров МЭИ (гл. ред. И. Н. Орлов) и др. 7 изд. 6 испр. и доп. М.: Энергоатомиздат, 1986. 712 с.