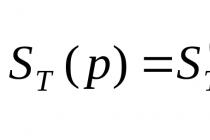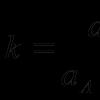^ मैट्रिक्स विधि
निर्देशित ग्राफ विधि के अलावा, रासायनिक प्रतिक्रियाओं की जटिल प्रणालियों के लिए स्टोइकोमेट्रिक समस्याओं को हल करने के अन्य तरीके भी हैं। मैट्रिक्स विधि आपको समस्या को एक ऐसे रूप में कम करने की अनुमति देती है जो कंप्यूटर तकनीक का उपयोग करके इसके आगे के समाधान के लिए सबसे उपयुक्त है।
आइए मैट्रिक्स विधि का उपयोग करके पिछली समस्या के समाधान पर विचार करें। 7 पदार्थ 4 रासायनिक प्रतिक्रियाओं की एक प्रणाली में भाग लेते हैं। इन पदार्थों को शामिल करने वाली रासायनिक प्रतिक्रियाओं के समीकरणों को ऐसे लिखा जा सकता है जैसे सभी पदार्थ एक साथ उनमें भाग लेते हैं। यदि कोई पदार्थ किसी रासायनिक प्रतिक्रिया में भाग नहीं लेता है, तो औपचारिक रूप से इसका मतलब है कि इस पदार्थ का स्टोइकोमेट्रिक गुणांक शून्य है। आइए हम इस बात से भी सहमत हों कि प्रारंभिक पदार्थों के लिए स्टोइकोमेट्रिक गुणांक को सकारात्मक माना जाएगा, और उत्पादों के लिए - नकारात्मक। फिर पिछले उदाहरण में मानी गई रासायनिक प्रतिक्रियाओं की प्रणाली के पहले रासायनिक समीकरणों को निम्नानुसार लिखा जा सकता है:
ए + 2 बी - 2 सी + 0 डी + 0 ई + 0 एफ + 0 एच = 0।
सभी पदार्थों और सभी प्रतिक्रियाओं के लिए समान रूप से तर्क करते हुए, हम प्रतिक्रियाओं में भाग लेने वाले सभी पदार्थों के द्रव्यमान के अनुपात का वर्णन करने वाले रैखिक समीकरणों की एक प्रणाली तैयार करेंगे। प्रणाली का आयाम 4x7 है, जहां 4 समीकरणों की संख्या है, 7 रासायनिक प्रतिक्रियाओं में भाग लेने वाले पदार्थों की संख्या है। इन समीकरणों के गुणांकों का मैट्रिक्स नीचे दिखाया गया है, और कॉलम वेक्टर शून्य है।
समीकरणों की परिणामी प्रणाली में, कई और समीकरणों को जोड़ना आवश्यक है जिनमें एक गैर-शून्य दाहिनी ओर है। ये समीकरण समस्या की प्रारंभिक स्थितियों के आधार पर लिखे गए हैं।
ए बी सी डी ई एफ एच
1 2 -2 0 0 0 0 0
1 0 0 -2 0 0 0 0
0 0 1 -1 0 -1 0 0
0 0 0 1 0 -2 -1 0
कुछ शर्तों के तहत, जब सिस्टम के कुछ घटकों के प्रारंभिक और वर्तमान द्रव्यमान के मूल्यों को जाना जाता है, तो रैखिक बीजगणित के तरीकों से एकल समाधान प्राप्त करना संभव है।
व्यावहारिक दृष्टिकोण से रासायनिक प्रतिक्रियाओं के स्टोइकोमेट्री की गणना करके प्रणालियों का विवरण सभी भाग लेने वाले पदार्थों के द्रव्यमान की गणना करना संभव बनाता है। इस प्रकार, सिस्टम के व्यवहार, उत्पादों की संरचना, उपभोग किए गए पदार्थों की मात्रा की भविष्यवाणी करना संभव है।
स्टोइकोमेट्रिक गणना यह मानती है कि किसी तकनीकी प्रक्रिया में सभी रासायनिक प्रतिक्रियाएं दाईं ओर जाती हैं।
^ रासायनिक प्रतिक्रिया प्रणालियों में संतुलन मॉडलिंग
अलौह धातु विज्ञान में तकनीकी प्रक्रियाओं की मुख्य सामग्री बनाने वाली रासायनिक प्रतिक्रियाओं का एक महत्वपूर्ण हिस्सा प्रतिवर्ती है। एक प्रतिवर्ती रासायनिक प्रतिक्रिया के उदाहरण पर विचार करें:
इस तरह की रासायनिक प्रतिक्रिया में संतुलन शामिल पदार्थों की गतिविधियों के कुछ मूल्यों पर प्राप्त किया जाता है। यदि ये पदार्थ घोल में हैं, और उनकी सांद्रता कम (पतला घोल) है, तो कुछ सन्निकटन के साथ, गतिविधि मूल्यों के बजाय, एकाग्रता मूल्यों का उपयोग किया जा सकता है। एक रासायनिक प्रतिक्रिया में संतुलन संतुलन स्थिरांक के मूल्य की विशेषता है:
 .
.
संतुलन स्थिरांक का मान गिब्स ऊर्जा में परिवर्तन के साथ जुड़ा हुआ है और इसमें शामिल पदार्थों के थर्मोडायनामिक डेटा से गणना की जा सकती है:

कहां Δ जी टी- दी गई रासायनिक प्रतिक्रिया के लिए गिब्स ऊर्जा में परिवर्तन, टी- तापमान, आरएक सार्वत्रिक गैस नियतांक है।
किसी दिए गए तापमान पर होने वाली रासायनिक प्रतिक्रिया के लिए संतुलन स्थिरांक के मूल्य की गणना करने के बाद, प्रारंभिक पदार्थों और उत्पादों की सांद्रता के अनुपात को निर्धारित करना संभव है, जो संतुलन तक पहुंचने पर स्थापित किया जाएगा।
एक प्रणाली की संतुलन संरचना को निर्धारित करना कुछ अधिक कठिन है जिसमें कई प्रतिवर्ती रासायनिक प्रतिक्रियाएं एक साथ होती हैं। निम्नलिखित उदाहरण पर विचार करें। पदार्थ ए, बी, सी, और डी को शामिल करने वाली प्रतिवर्ती रासायनिक प्रतिक्रियाओं की एक प्रणाली होने दें। इस प्रणाली में, पदार्थ ए क्रमिक रूप से और विपरीत रूप से पदार्थ सी में परिवर्तित हो जाता है, प्रारंभिक रूप से बी बनाता है। एक समानांतर पथ भी संभव है: पदार्थ ए, में बी के गठन के समानांतर, डी बनाने के लिए विघटित होता है। दी गई शर्तों (तापमान, दबाव) के तहत, सिस्टम में संतुलन स्थापित किया जाएगा और पदार्थों की संतुलन सांद्रता प्राप्त की जाएगी।
संतुलन सांद्रता की गणना करने के लिए, हम संतुलन सांद्रता के संदर्भ में सभी प्रतिक्रियाओं के संतुलन स्थिरांक के लिए व्यंजक लिखते हैं:
ए बी  ;
; 
बी सी  ;
;
ए डी  ;
;  .
.
प्रारंभिक क्षण में कोई मध्यवर्ती पदार्थ B और C न होने दें, साथ ही अंतिम उत्पाद D:
 ; सी बी0 = 0; 0 = 0; सी डी 0 = 0।
; सी बी0 = 0; 0 = 0; सी डी 0 = 0।
थर्मोडायनामिक डेटा का उपयोग करके प्रत्येक प्रतिक्रिया के लिए संतुलन स्थिरांक के मूल्यों की गणना की जाती है:  ... इस प्रकार, संतुलन स्थिरांक के मानों को ज्ञात मान माना जाएगा।
... इस प्रकार, संतुलन स्थिरांक के मानों को ज्ञात मान माना जाएगा।
इस प्रणाली की प्रति इकाई आयतन, C A0 - CA घटक A के उपभोग किए गए मोल की संख्या है। रासायनिक प्रतिक्रियाओं के स्टोइकोमेट्री और पदार्थ के संरक्षण के नियम के अनुसार, द्रव्यमान A का नुकसान द्रव्यमान के योग के बराबर है परिणामी पदार्थ बी, सी और डी, जिसे समीकरण द्वारा व्यक्त किया जा सकता है:
सी ए0 - सी ए = सी बी + सी सी + सी डी।
हम समीकरण को निम्नलिखित रूप में बदलते हैं:
सी ए0 = सी ए + सी बी + सी सी + सी डी,
और हम व्यंजक के दायीं ओर पदार्थों के संगत सांद्रण को प्रतिस्थापित करते हैं:
सी ए0 = सी ए + के 1 सी ए + के 1 के 2 सी ए + के 3 सी ए।
हम समीकरण के सजातीय पदों को समूहित करते हैं
सी ए 0 = सी ए (1 + के 1 + के 1 के 2 + के 3)
और हमें संतुलन सांद्रता C A के लिए व्यंजक प्राप्त होता है
 .
.
अन्य पदार्थों की संतुलन सांद्रता निर्धारित करना आसान है, क्योंकि सभी संतुलन स्थिरांक के मान हमें पिछली गणना से ज्ञात हैं, और भावों में सीए होता है।
रासायनिक प्रतिक्रियाओं की प्रणालियों में संतुलन की गणना करते समय, प्रत्येक प्रतिक्रिया के k p को जानना आवश्यक है, प्रणाली की प्रारंभिक संरचना - इससे प्रणाली की संतुलन संरचना की गणना करना संभव हो जाता है।
सिस्टम की संतुलन संरचना की गणना की वास्तविक समस्याएं बहुत अधिक जटिल हैं: इन समस्याओं में समीकरण अरेखीय हैं; यह ध्यान रखना आवश्यक है कि प्रतिक्रिया में प्रवेश करने वाले घटक विभिन्न चरणों में हैं; सांद्रता के बजाय, घटकों की गतिविधियों के मूल्यों का उपयोग करना सही है। इस तरह की जटिल प्रणालियों में संतुलन की गणना का व्यावहारिक अर्थ इस तथ्य से उबलता है कि प्रणाली की गणना की गई संतुलन संरचना भौतिक-रासायनिक सीमा है जो एक वास्तविक प्रक्रिया तक पहुंच सकती है यदि इसके कार्यान्वयन के लिए असीमित समय आवंटित किया जाता है।
^ रासायनिक प्रतिक्रियाओं के कैनेटीक्स की मॉडलिंग
भौतिक रसायन विज्ञान में, रासायनिक प्रतिक्रिया की दर समीकरण के अनुसार निर्धारित की जाती है:
 ,
,
कहां डीक्यू- अभिकारक के द्रव्यमान में परिवर्तन, मोल।
डीटी- समय वृद्धि, एस।
वीप्रतिक्रिया स्थान का एक उपाय है।
सजातीय रासायनिक प्रतिक्रियाओं के बीच अंतर करें जिसमें शामिल सभी पदार्थ एक ही चरण (गैस या तरल) के भीतर हों। ऐसी प्रतिक्रियाओं के लिए, प्रतिक्रिया स्थान का माप मात्रा है, और वेग का आयाम होगा:  .
.
विभिन्न चरणों (गैस-ठोस, गैस-तरल, तरल-तरल, ठोस-तरल) में पदार्थों के बीच विषम रासायनिक प्रतिक्रियाएं होती हैं। इस मामले में, वास्तविक रासायनिक प्रतिक्रिया इंटरफ़ेस पर महसूस की जाती है, जो प्रतिक्रिया स्थान का एक उपाय है।
विषम प्रतिक्रियाओं के लिए, दर का आयाम अलग है:  .
.
प्रतिक्रियाशील पदार्थों के द्रव्यमान में परिवर्तन का अपना संकेत होता है। प्रारंभिक पदार्थों के लिए, प्रतिक्रिया के दौरान द्रव्यमान कम हो जाता है, द्रव्यमान में परिवर्तन का नकारात्मक संकेत होता है, और वेग का परिमाण ऋणात्मक मान लेता है। रासायनिक प्रतिक्रिया के उत्पादों के लिए, द्रव्यमान बढ़ता है, द्रव्यमान में परिवर्तन सकारात्मक होता है, और वेग का संकेत भी सकारात्मक माना जाता है।
एक साधारण रासायनिक प्रतिक्रिया पर विचार करें
ए + 2 बी = 2 सी।
सरल प्रतिक्रियाओं में वे शामिल हैं जो एक चरण में किए जाते हैं और अंत तक जाते हैं, अर्थात। अपरिवर्तनीय हैं।
आइए ऐसी रासायनिक प्रतिक्रिया की दर निर्धारित करें। इसके लिए सबसे पहले यह तय करना आवश्यक है कि किन पदार्थों की प्रतिक्रिया दर निर्धारित की जाएगी: आखिरकार, ए और बी प्रारंभिक पदार्थ हैं, और उनके द्रव्यमान में परिवर्तन नकारात्मक है, और सी अंतिम उत्पाद है, और इसका द्रव्यमान समय के साथ बढ़ता जाता है। इसके अलावा, प्रतिक्रिया में सभी स्टोइकोमेट्रिक गुणांक एकता के बराबर नहीं होते हैं, जिसका अर्थ है कि यदि प्रवाह दर ए कुछ समय के लिए 1 मोल के बराबर है, तो उसी समय के दौरान प्रवाह दर बी 2 मोल होगी, और, तदनुसार, A और B के द्रव्यमान में परिवर्तन से परिकलित दर मान आधे से भिन्न होंगे।
एक साधारण रासायनिक प्रतिक्रिया के लिए, दर का एक ही उपाय प्रस्तावित किया जा सकता है, जिसे निम्नानुसार निर्धारित किया जाता है:
 ,
,
कहां आर मैं- प्रतिक्रिया के i-वें प्रतिभागी की गति
एस मैंप्रतिक्रिया में i-वें प्रतिभागी का स्टोइकोमेट्रिक गुणांक है।
प्रारंभिक पदार्थों के लिए स्टोइकोमेट्रिक गुणांक को सकारात्मक माना जाता है, प्रतिक्रिया उत्पादों के लिए वे नकारात्मक होते हैं।
यदि प्रतिक्रियाएं एक अलग प्रणाली में होती हैं जो बाहरी वातावरण के साथ पदार्थ का आदान-प्रदान नहीं करती है, तो केवल एक रासायनिक प्रतिक्रिया से सिस्टम में पदार्थ के द्रव्यमान में परिवर्तन होता है, और इसके परिणामस्वरूप, उनकी सांद्रता में। ऐसी प्रणाली में, एकाग्रता में परिवर्तन का एकमात्र कारण है साथएक रासायनिक प्रतिक्रिया है। इस विशेष मामले के लिए
 ,
,
एक रासायनिक प्रतिक्रिया की दर शामिल पदार्थों की सांद्रता और तापमान पर निर्भर करती है।

कहां क - एक रासायनिक प्रतिक्रिया की दर स्थिर, साथ ए ,साथ वी- पदार्थों की एकाग्रता, एन 1 , एन 2 - संबंधित पदार्थों के लिए आदेश। इस अभिव्यक्ति को भौतिक रसायन विज्ञान में सामूहिक क्रिया के नियम के रूप में जाना जाता है।
सांद्रता मान जितना अधिक होगा, रासायनिक प्रतिक्रिया की दर उतनी ही अधिक होगी।
आदेश ( एन) प्रयोगात्मक रूप से निर्धारित किया जाता है और रासायनिक प्रतिक्रिया के तंत्र से जुड़ा होता है। आदेश एक पूर्णांक या भिन्नात्मक संख्या हो सकता है, कुछ पदार्थों के लिए शून्य-क्रम प्रतिक्रियाएं भी होती हैं। अगर आदेश है मैं-वाँ पदार्थ शून्य के बराबर है, तो रासायनिक प्रतिक्रिया की दर इस पदार्थ की सांद्रता पर निर्भर नहीं करती है।
रासायनिक प्रतिक्रिया की दर तापमान पर निर्भर करती है। अरहेनियस कानून के अनुसार, तापमान में बदलाव के साथ दर लगातार बदलती रहती है:

कहां ^ ए- पूर्व-घातीय कारक;
इ- सक्रियण ऊर्जा;
आर- सार्वभौमिक गैस स्थिरांक, स्थिरांक;
टी- तापमान।
साथ ही प्रतिक्रिया के क्रम की भयावहता, सक्रियण ऊर्जा के मूल्य और प्रीएक्सपोनेंशियल कारक एक विशेष प्रतिक्रिया के लिए प्रयोगात्मक रूप से निर्धारित किए जाते हैं।
यदि कोई रासायनिक अभिक्रिया विषमांगी प्रक्रिया में की जाती है, तो उसकी दर प्रारंभिक पदार्थों की आपूर्ति और रासायनिक प्रतिक्रिया क्षेत्र से उत्पादों को हटाने की प्रक्रिया से भी प्रभावित होती है। इस प्रकार, एक जटिल प्रक्रिया होती है जिसमें प्रसार चरण (आपूर्ति, निकासी) और गतिज चरण होते हैं - वास्तविक रासायनिक प्रतिक्रिया। पूरी प्रक्रिया की गति, प्रयोग में देखी गई, सबसे धीमी अवस्था की गति से निर्धारित होती है।
इस प्रकार, प्रक्रिया (मिश्रण) के प्रसार चरण की दर को प्रभावित करके, हम पूरी प्रक्रिया की दर को समग्र रूप से प्रभावित करते हैं। यह प्रभाव पूर्व-घातीय कारक ए के मूल्य को प्रभावित करता है।
अधिकांश रासायनिक प्रतिक्रियाएं सरल नहीं होती हैं (अर्थात, वे एक चरण में नहीं जाती हैं और न ही अंत तक) - जटिल रासायनिक प्रतिक्रियाएं:
ए) एबी - प्रतिवर्ती;
बी) ए → बी; В → - लगातार;
बी) ए → बी; ए → सी - समानांतर।
एक जटिल रासायनिक प्रतिक्रिया के लिए गति का कोई एकसमान माप नहीं है... सरल के विपरीत, यहां हम प्रत्येक रसायन के बनने और नष्ट होने की दर के बारे में बात कर सकते हैं। इस प्रकार, यदि निकाय में रासायनिक अभिक्रियाएँ होती हैं और एन प्रत्येक के लिए पदार्थ एनपदार्थों का अपना गति मान होता है।
किसी भी पदार्थ के लिए, गठन और विनाश की दर इस पदार्थ की भागीदारी के साथ सभी चरणों की दरों का बीजगणितीय योग है।
जटिल रासायनिक प्रतिक्रिया दर
आइए हम निम्नलिखित उदाहरण का उपयोग करके जटिल रासायनिक प्रतिक्रियाओं की एक प्रणाली के कैनेटीक्स को मॉडलिंग करने पर विचार करें। एक तकनीकी प्रक्रिया होने दें, जिसका सार निम्नलिखित रासायनिक प्रतिक्रियाओं द्वारा प्रदर्शित किया जाता है:
कश्मीर 1; 1 से बी
कश्मीर 2; 0.7 से सी
कश्मीर 3; 1 से ए; 0.35 एन . में
कश्मीर 4; 1 से सी; 1 से डी
कश्मीर 5; 2 से ई;
आर ए = -के 1 सी बी + के 2 सी सी 0.7 - के 3 सी ए सी एच 0.35
आर बी= -2k 1 सी बी + 2k 2 सी सी 0.7
आर सी = के 1 सी बी - के 2 सी सी 0.7 - के 4 सी सी सी डी + के 5 सी ई 2
आर डी = के 3 सी ए सी एच 0.35 - के 4 सी सी सी डी + के 5 सी ई 2
आर ई = के 4 सी सी सी डी - 3k 5 सी ई 2
काइनेटिक स्थिरांक (पदार्थों के क्रम और चरणों के लिए दर स्थिरांक के मान) प्रयोगात्मक रूप से निर्धारित किए गए थे। चरणों के अनुरूप तीरों के ऊपर प्रक्रिया आरेख में, पदार्थों के क्रम के परिमाण दिखाए जाते हैं। अनिर्दिष्ट आदेश शून्य हैं।
6 पदार्थ प्रक्रिया में भाग लेते हैं: ए और बी प्रारंभिक हैं, सी और डी मध्यवर्ती हैं, ई अंतिम उत्पाद है, एच चरणों में से एक का उत्प्रेरक है। तीन रासायनिक प्रतिक्रियाओं में पाँच चरण होते हैं, जिनमें से तीन प्रत्यक्ष होते हैं और दो विपरीत होते हैं।
सभी प्रतिक्रियाओं को एकरूपता से किया जाता है और पदार्थ में बंद प्रणाली में होता है, जो दर को चिह्नित करने के लिए निम्नलिखित अभिव्यक्तियों का उपयोग करने का कारण देता है:
 .
.
उपरोक्त के आधार पर, हम प्रत्येक पदार्थ-प्रतिभागी के लिए वेगों के व्यंजक लिखेंगे। कुल मिलाकर, हमें पदार्थों की संख्या के लिए 6 व्यंजक मिलते हैं। प्रत्येक पदार्थ के लिए, खपत या गठन की दर किसी दिए गए पदार्थ की भागीदारी के साथ सभी चरणों की दरों का बीजगणितीय योग है। तो, पदार्थ ए तीन चरणों में भाग लेता है, पहले में एक प्रारंभिक पदार्थ के रूप में, दूसरे में एक उत्पाद के रूप में, तीसरे में फिर से एक प्रारंभिक पदार्थ के रूप में। पहले और तीसरे चरण के लिए गति की शर्तें नकारात्मक होंगी, दूसरे चरण के लिए गति का सकारात्मक संकेत होगा। प्रत्येक चरण के लिए दर मान, प्रभावी द्रव्यमान के नियम के अनुसार, संबंधित चरण की दर स्थिरांक और पदार्थों में परिमाण के क्रम के बराबर शक्तियों में पदार्थों की सांद्रता के उत्पाद हैं। इसे ध्यान में रखते हुए, पदार्थों की गति के लिए व्यंजक इस प्रकार होंगे:
 = -के 1 सी बी + के 2 सी सी 0.7 - के 3 सी ए सी एच 0.35
= -के 1 सी बी + के 2 सी सी 0.7 - के 3 सी ए सी एच 0.35
 = -2k 1 सी बी + 2k 2 सी सी 0.7
= -2k 1 सी बी + 2k 2 सी सी 0.7
 = के 1 सी बी - के 2 सी सी 0.7 - के 4 सी सी सी डी + के 5 सी ई 2
= के 1 सी बी - के 2 सी सी 0.7 - के 4 सी सी सी डी + के 5 सी ई 2
 = के 3 सी ए सी एच 0.35 - के 4 सी सी सी डी + के 5 सी ई 2
= के 3 सी ए सी एच 0.35 - के 4 सी सी सी डी + के 5 सी ई 2
 = 3k 4 सी सी सी डी - 3k 5 सी ई 2
= 3k 4 सी सी सी डी - 3k 5 सी ई 2
 = 0.
= 0.
तीसरे चरण उत्प्रेरक पदार्थ एच के लिए अंतिम दर शून्य है। प्रतिक्रिया के दौरान उत्प्रेरक का द्रव्यमान नहीं बदलता है।
सभी समीकरणों के बाईं ओर, समय के संबंध में पदार्थ की सांद्रता का व्युत्पन्न होता है, इसलिए गतिकी के समीकरण अंतर होते हैं। एक मनमाना समय पर समीकरणों के दाहिने हाथ की सांद्रता को एक साथ सभी समीकरणों को संतुष्ट करना चाहिए, जिसका अर्थ है कि गणितीय अर्थों में गतिज समीकरणों का सेट समीकरणों की एक प्रणाली है।
रासायनिक कैनेटीक्स मॉडल अंतर समीकरणों की एक प्रणाली है, जिसका समाधान कार्यों का एक सेट है सी मैं = एफ मैं (टी) :
सी ए = एफ 1 (टी)
कार्यों के एक विशिष्ट रूप को स्थापित करने के लिए, अंतर समीकरणों की एक प्रणाली को हल करना आवश्यक है, अर्थात। गतिज समीकरणों की प्रणाली को एकीकृत करें। हम एक सरल उदाहरण का उपयोग करके नीचे गतिकी के समीकरणों के एकीकरण पर विचार करेंगे, और उसके बाद हम ऊपर दी गई समस्या पर लौटेंगे।
^ गतिज समीकरणों का एकीकरण
पदार्थ ए के अपघटन की रासायनिक प्रतिक्रिया होने दें, जिसके परिणामस्वरूप पदार्थ बी बनता है। यह प्रयोगात्मक रूप से स्थापित किया गया है कि इसका एकाग्रता ए में पहला क्रम है, और इसके कार्यान्वयन की शर्तों के लिए स्थिर दर का मूल्य है k के बराबर है। इसे नीचे प्रतिक्रिया आरेख में दर्शाया गया है।
क; 1 से ए
प्रतिक्रिया दर r a = –kC A, or . है
 .
.
आइए गतिकी के अवकल समीकरण को हल करने के लिए प्रारंभिक शर्तों को परिभाषित करें। हम मान लेंगे कि प्रतिक्रिया के प्रारंभिक क्षण में हम पदार्थ ए की एकाग्रता को जानते हैं, हम इसे सी एओ के रूप में नामित करेंगे। हम प्रारंभिक शर्तों को फॉर्म में लिखते हैं  ... हम सीमा के प्रतिस्थापन के साथ इंटीग्रल का उपयोग करके परिणामी समीकरण को एकीकृत करेंगे। एकीकरण की सीमाएं प्रारंभिक स्थितियों से निर्धारित होती हैं: जब समय शून्य होता है, तो एकाग्रता ए प्रारंभिक एक के बराबर होती है, एक मनमाना क्षण पर टीएकाग्रता है साथ ए :
... हम सीमा के प्रतिस्थापन के साथ इंटीग्रल का उपयोग करके परिणामी समीकरण को एकीकृत करेंगे। एकीकरण की सीमाएं प्रारंभिक स्थितियों से निर्धारित होती हैं: जब समय शून्य होता है, तो एकाग्रता ए प्रारंभिक एक के बराबर होती है, एक मनमाना क्षण पर टीएकाग्रता है साथ ए :
 .
.
एकीकरण के परिणामस्वरूप, हमारे पास है:
 ,
,
लघुगणक के अंतर को भागफल के लघुगणक से प्रतिस्थापित करते हुए, हमारे पास आगे है:
 ,
,
पोटेंशिएशन को पूरा करते हुए, हम प्राप्त करते हैं:
 .
.
सभी परिवर्तनों के बाद, अंतर समीकरण का समाधान एक घातीय घटते कार्य है:
 .
.
आइए देखें कि क्या प्राप्त समाधान हमारी समस्या की शर्तों के विपरीत है। पर टी= 0, यानी एक रासायनिक प्रतिक्रिया की शुरुआत में साथ ए = सी ए 0 क्योंकि घातांक एक हो जाता है। दरअसल, प्रारंभिक क्षण में, पदार्थ A की सांद्रता प्रारंभिक एक के बराबर होती है। पर टी→ ऋणात्मक घातांक वाला घातांक परिमाण में शून्य हो जाता है। एक असीम रूप से लंबे समय तक, एक रासायनिक प्रतिक्रिया के कारण, सभी पदार्थ विघटित हो जाते हैं और V का निर्माण करते हैं।
^ संख्यात्मक एकीकरण के तरीके
आइए अब पिछली समस्या पर वापस आते हैं। यह स्पष्ट है कि अवकल समीकरणों की एक प्रणाली का एकीकरण पहले की तुलना में अधिक कठिन कार्य है। एकीकरण के विश्लेषणात्मक तरीकों का उपयोग शायद ही संभव है, क्योंकि अंतर समीकरणों के दाहिने हाथ में एक साथ कई पदार्थों की सांद्रता होती है, और चर को अलग करना संभव नहीं होगा।
आइए संख्यात्मक एकीकरण विधि का उपयोग करें। ऐसा करने के लिए, हम समय अक्ष को छोटे खंडों (चरणों) में विभाजित करेंगे। यह मानते हुए कि पदार्थों की सांद्रता का समय व्युत्पन्न समय वृद्धि के लिए एकाग्रता वृद्धि के अनुपात की गणितीय सीमा है, पर Δ टी , शून्य की ओर झुकाव:
 ,
,
हम अवकल समीकरणों की प्रणाली को बीजीय समीकरणों की प्रणाली में बदल देते हैं। बाईं ओर, हम समय वृद्धि को जानते हैं, क्योंकि हम समय को स्वयं चुनते हैं। केवल महत्वपूर्ण बात यह है कि यह कदम छोटा होना चाहिए।
दाईं ओर, हम प्रयोग से सभी दर स्थिरांक के मूल्यों को भी जानते हैं, आदेशों के परिमाण के बारे में भी यही कहा जाना चाहिए। हम प्रारंभिक स्थितियों का उपयोग करते हुए, दाहिने हाथ में सभी पदार्थों की सांद्रता के मूल्यों को भी प्रतिस्थापित करते हैं। सिस्टम के प्रत्येक समीकरण में इस मामले में केवल एक अज्ञात मात्रा होती है - एकाग्रता में परिवर्तन Δ सी मैं... वास्तव में, यह समाधान के पहले चरण के लिए एकाग्रता में परिवर्तन है, जब समय शून्य से (रासायनिक प्रतिक्रिया की शुरुआत) से बदल जाता है Δ टी. अपने स्वयं के संकेत के साथ एकाग्रता में परिवर्तन को प्रारंभिक एकाग्रता के साथ अभिव्यक्त किया जाता है और समाधान के पहले चरण के अंत में प्रत्येक पदार्थ की एकाग्रता निर्धारित की जाती है।
समाधान के अगले चरण में, हम समाधान के पिछले चरण से दाहिनी ओर एकाग्रता मूल्यों को प्रतिस्थापित करते हैं और फिर से प्राप्त करते हैं Δ सी मैंलेकिन अब समाधान के अगले चरण के लिए, जैसा कि चित्र में दिखाया गया है।
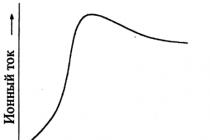
विलयन के प्रत्येक चरण पर, हमें अभिक्रियाओं में भाग लेने वाले सभी पदार्थों की सांद्रता में परिवर्तन के अनुरूप निर्देशांक प्राप्त होते हैं। बिंदुओं का स्थान, जो निर्देशांक हैं, प्रत्येक पदार्थ के लिए समय के साथ एकाग्रता परिवर्तन फ़ंक्शन का एक ग्राफ देगा। ध्यान दें कि संख्यात्मक एकीकरण के परिणामस्वरूप, हमें एक विश्लेषणात्मक अभिव्यक्ति नहीं मिलती है जो समय के साथ एकाग्रता में परिवर्तन को निर्दिष्ट करती है, ग्राफ पर निर्देशांक गणना द्वारा प्राप्त किए जाते हैं। हालांकि, समय के साथ एकाग्रता में परिवर्तन के कार्यों के रेखांकन का निर्माण संभव है, और वक्रों का आकार हमें कई निष्कर्ष निकालने की अनुमति देता है जिनका व्यावहारिक अर्थ है।
यह स्पष्ट है कि प्रारंभिक पदार्थों की सांद्रता समय के साथ घटती जाती है, क्योंकि वे प्रतिक्रिया में भस्म हो जाते हैं। यह कम स्पष्ट नहीं है कि अंतिम उत्पादों की सांद्रता बढ़ रही है।
मध्यवर्तियों का व्यवहार एक अलग विचार के योग्य है। मध्यवर्ती पदार्थों के सांद्रण ग्राफ में एक निश्चित प्रतिक्रिया समय के अनुरूप मैक्सिमा होता है। यदि मध्यवर्ती पदार्थ रासायनिक प्रतिक्रियाओं का लक्ष्य उत्पाद है, तो अधिकतम एकाग्रता इस लक्ष्य पदार्थ को प्राप्त करने के लिए इष्टतम अवधि से मेल खाती है।
ऐसा इसलिए है क्योंकि रासायनिक प्रतिक्रिया के प्रारंभिक क्षण में, प्रारंभिक पदार्थों की सांद्रता अधिक होती है, और प्रारंभिक पदार्थों की भागीदारी के साथ रासायनिक प्रतिक्रिया की दर उनकी सांद्रता के समानुपाती होती है। प्रारंभिक सामग्री से जुड़ी प्रतिक्रियाएं शुरू में उच्च दरों पर होती हैं। इसका मतलब है कि मध्यवर्ती पदार्थ भी उच्च दर पर बनते हैं।
दूसरी ओर, मध्यवर्ती पदार्थों के अपघटन की दर भी उनकी सांद्रता के समानुपाती होती है, और शुरुआत में छोटी होती है। मध्यवर्ती पदार्थों के गठन की दर उनके अपघटन की दर से अधिक होती है, जो मध्यवर्ती पदार्थों के संचय में योगदान करती है, उनकी एकाग्रता बढ़ जाती है।
जैसे-जैसे रासायनिक प्रतिक्रिया विकसित होती है, मध्यवर्ती पदार्थों के बनने की दर कम होती जाती है और उनके विनाश की दर बढ़ जाती है। जब वेगों का मान समान हो जाता है, तो सांद्रता में वृद्धि रुक जाती है, और सिस्टम में मध्यवर्ती पदार्थ की अधिकतम सांद्रता देखी जाती है।
इसके अलावा, मध्यवर्ती के गठन की दर कम हो जाती है क्योंकि प्रारंभिक सामग्री की एकाग्रता में कमी जारी रहती है। मध्यवर्ती पदार्थ के विनाश की दर भी कम हो जाती है, गठन की दर से अधिक परिमाण में शेष रहती है, और इससे सिस्टम में मध्यवर्ती पदार्थ की खपत होती है और इसकी एकाग्रता में गिरावट आती है।

 ;
;
टीसी पदार्थ सी प्राप्त करने का इष्टतम समय है।
पदार्थ C के व्यवहार पर विचार करें: समय के प्रारंभिक क्षण में C C = 0।
के 1 सी बी> के 2 सी सी 0.7
इस प्रकार, कैनेटीक्स का मॉडलिंग रासायनिक प्रतिक्रियाओं की प्रणालियों में सभी पदार्थों के गठन और खपत को निर्धारित करना संभव बनाता है, समय के एक समारोह के रूप में एकाग्रता समारोह के रूप को स्थापित करने के लिए, और कुछ मामलों में रासायनिक संचालन के लिए इष्टतम स्थितियों का निर्धारण करने के लिए। प्रतिक्रिया।
^ पदार्थ के प्रवाह में रासायनिक प्रतिक्रियाएं
कई तकनीकी उपकरण निरंतर मोड में काम करते हैं। आइए, एक उदाहरण के रूप में, तांबे के सांद्र और फ्लक्स से चार्ज को संसाधित करने के लिए एक पिघलने वाली भट्टी पर विचार करें। ऐसे उपकरण का आरेख नीचे चित्र में दिखाया गया है।
एच  एक सतत फ्लो-थ्रू उपकरण एक फ्लो-थ्रू रिएक्टर है जिसमें रासायनिक प्रतिक्रियाओं का एक निश्चित सेट किया जाता है।
एक सतत फ्लो-थ्रू उपकरण एक फ्लो-थ्रू रिएक्टर है जिसमें रासायनिक प्रतिक्रियाओं का एक निश्चित सेट किया जाता है।
पदार्थ प्रवाह की उपस्थिति रासायनिक प्रतिक्रियाओं को अंजाम देने की स्थितियों को प्रभावित करती है।
पदार्थ के वास्तविक प्रवाह में जटिल गुण होते हैं:
हाइड्रोडायनामिक शासन - लामिना, अशांत, क्षणिक;
चरणों की संख्या - बहु- और एकल-चरण।
एक उदाहरण एक पाइप के माध्यम से चलने वाली धारा है। एक खंड के भीतर प्रवाह की गति समान नहीं है: गति का उच्चतम मूल्य प्रवाह की धुरी पर होता है, और दीवारों के पास चिपचिपाहट की ताकतों द्वारा प्रवाह की मंदी के कारण, यह गति शून्य से थोड़ा भिन्न होती है . हालांकि, यदि प्रवाह माध्यम की वॉल्यूमेट्रिक प्रवाह दर क्यू है और क्रॉस-अनुभागीय क्षेत्र एफ है, तो प्रवाह की औसत प्रवाह दर क्यू / एफ के बराबर निर्धारित करना आसान है।
 क्यू एम 3 / एस
क्यू एम 3 / एस

मल्टीफ़ेज़ प्रवाह का वर्णन करते समय और भी कठिनाइयाँ उत्पन्न होती हैं, और वास्तविक प्रवाह सबसे अधिक बार वे होते हैं।
इस संबंध में, गणितीय मॉडल बनाते समय वास्तविक प्रवाह के गुणों को ध्यान में रखना मुश्किल है। इसलिए, प्रवाह के माध्यम से उपकरण का एक मॉडल बनाने के लिए, प्रवाह के प्रवाह के कई आदर्श मॉडल हैं।
^ 1. प्लग-फ्लो मॉडल - ऐसा आदर्श प्रवाह मॉडल निम्नलिखित मान्यताओं पर आधारित है (इस प्रकार का उपकरण एक ट्यूबलर भट्ठा हो सकता है):
प्रवाह स्थिर है, माध्यम की वॉल्यूमेट्रिक प्रवाह दर समय के साथ नहीं बदलती है;

ऐसी धारा में, धारा के सभी बिंदुओं पर वेग समान होते हैं;
इस तरह के प्रवाह में वॉल्यूम डीवी का एक तत्व पदार्थ में बंद प्रणाली है (पड़ोसी तत्वों के साथ आदान-प्रदान नहीं करता है);
प्लग प्रवाह में कोई अनुदैर्ध्य मिश्रण नहीं होता है;
प्रवाह में कोई क्रॉस मिक्सिंग भी नहीं है।
प्लग प्रवाह के मामले में कैनेटीक्स मॉडलिंग के लिए, पदार्थ में पृथक प्रणालियों के लिए लागू एक दृष्टिकोण काफी उपयुक्त है।
विस्थापन तंत्र में होने वाली प्रथम कोटि की अभिक्रिया पर विचार कीजिए।
कश्मीर 1; 1 से ए
साथ  आइए एक मॉडल बनाएं जो हमें आउटपुट एकाग्रता ए की गणना करने की अनुमति देता है। स्थिरांक ज्ञात है, पहला क्रम।
आइए एक मॉडल बनाएं जो हमें आउटपुट एकाग्रता ए की गणना करने की अनुमति देता है। स्थिरांक ज्ञात है, पहला क्रम।



 - तंत्र में पदार्थ का निवास समय
- तंत्र में पदार्थ का निवास समय


दर स्थिरांक जितना बड़ा होगा क, उतनी ही तेजी से एकाग्रता निकास बिंदु पर एकाग्रता की ओर प्रवृत्त होती है।
विस्थापन तंत्र के भीतर पदार्थ की सांद्रता स्थिर नहीं रहती है - यह प्रवेश बिंदु पर एकाग्रता से निकास बिंदु पर एकाग्रता तक गिरती है।
^ 2. सही मिश्रण का मॉडल (इस प्रकार का एक उपकरण है, उदाहरण के लिए, एक केएस भट्टी, एक हाइड्रोमेटालर्जिकल लीचिंग रिएक्टर, आदि)।
धारणाएं:
प्रवाह स्थिर है, उपकरण के माध्यम से पदार्थ (क्यू) की वॉल्यूमेट्रिक प्रवाह दर स्थिर होनी चाहिए;
आदर्श मिश्रण उपकरण के सभी बिंदुओं पर सांद्रता समान होती है।
 दूसरी धारणा का एक परिणाम यह है कि निकास बिंदु पर पदार्थ की एकाग्रता तंत्र के अंदर की एकाग्रता के बराबर होती है।
दूसरी धारणा का एक परिणाम यह है कि निकास बिंदु पर पदार्थ की एकाग्रता तंत्र के अंदर की एकाग्रता के बराबर होती है। 
तंत्र में किसी पदार्थ का औसत निवास समय -  .
.
एक आदर्श मिश्रण उपकरण में प्रवाह के विभिन्न भागों का निवास समय समान नहीं होता है।
ऐसे उपकरण में आयतन तत्व एक खुली प्रणाली है, ऐसे उपकरण के लिए एक बंद प्रणाली के लिए दृष्टिकोण उपयुक्त नहीं है। इस मामले में कैनेटीक्स का वर्णन करने के लिए, हम पदार्थ के नियम का उपयोग करते हैं और पूरे उपकरण पर विचार करते हैं, सभी बिंदुओं पर एकाग्रता समान होती है। पदार्थ के संरक्षण के नियम के आधार पर, हम पूरे तंत्र के लिए भौतिक संतुलन समीकरण को संपूर्ण (प्रति इकाई समय) के रूप में लिखते हैं:
आय - खपत = 0
एक आदर्श मिश्रण उपकरण की शर्तों के तहत पहले क्रम की अपघटन प्रतिक्रिया होने दें:
कश्मीर 1; 1 से ए
पदार्थ A के लिए भौतिक संतुलन घटकों का योग होगा:
1 पद - समय की प्रति इकाई प्रवाह द्वारा शुरू किए गए पदार्थ ए के मोल की संख्या;
2 अवधि - समय की प्रति इकाई तंत्र से पदार्थ का प्रवेश;
3 पद - रासायनिक प्रतिक्रिया में खपत पदार्थ का द्रव्यमान। हम समीकरण के दोनों पक्षों को वॉल्यूमेट्रिक प्रवाह दर क्यू 0 से विभाजित करते हैं:

 .
.
आइए हम दोनों उपकरणों में रासायनिक प्रतिक्रियाओं के लिए समान स्थितियां बनाएं (समान तापमान,  के 1 = के 2)। आइए मान लें कि एक निश्चित तापमान पर के 1 = के 2 = 1। सी ए0 = 1 मोल / मी 3 सेट करें। वीए = 1 एम 3, क्यू 1 = क्यू 2 = 1 एम 3 / एस। फिर:
के 1 = के 2)। आइए मान लें कि एक निश्चित तापमान पर के 1 = के 2 = 1। सी ए0 = 1 मोल / मी 3 सेट करें। वीए = 1 एम 3, क्यू 1 = क्यू 2 = 1 एम 3 / एस। फिर:

 .
.
हैरानी की बात यह है कि एक ही रासायनिक प्रतिक्रिया का परिणाम अलग-अलग उपकरणों में अलग-अलग होता है। एक प्लग फ्लो उपकरण अधिक प्रभावी होता है, जिसमें आउटलेट की सांद्रता कम होती है।
इसका कारण रासायनिक प्रतिक्रिया की दर नहीं है (यह दोनों उपकरणों में समान है), बल्कि प्रवाह तत्वों के मिश्रण की उपस्थिति या अनुपस्थिति है। आदर्श मिश्रण के उपकरण में, आउटलेट पर एकाग्रता स्थापित की जाएगी, जो कि पदार्थ के उन हिस्सों को मिलाने का परिणाम है जो अलग-अलग समय के लिए डिवाइस के अंदर थे। पदार्थ के कुछ हिस्से उपकरण को जल्दी से छोड़ देते हैं, और ऐसे हिस्सों में प्रतिक्रिया समय कम होता है, जबकि पदार्थ ए की एकाग्रता, इसके विपरीत, अधिक होती है। पदार्थ के अन्य भाग लंबे समय तक तंत्र के अंदर रहते हैं, रासायनिक प्रतिक्रिया की अवधि लंबी होती है, और ए की अवशिष्ट सांद्रता छोटी होती है।
^ सेलुलर प्रवाह मॉडल ... इस मॉडल के अनुसार, एक वास्तविक तकनीकी उपकरण को एक आदर्श योजना से बदल दिया जाता है - आदर्श मिश्रण की कोशिकाओं का एक क्रम।
 1 ; 1 से ए
1 ; 1 से ए एन एस  मुंह n = 2, फिर पहली सेल के आउटपुट पर:
मुंह n = 2, फिर पहली सेल के आउटपुट पर: 

अगर n सेल, तो 
उस पर विचार करना  - हम आदर्श विस्थापन तंत्र के समाधान के लिए पास करते हैं। एन = 1 के लिए, हमारे पास आदर्श मिश्रण उपकरण के लिए एक स्पष्ट समाधान है।
- हम आदर्श विस्थापन तंत्र के समाधान के लिए पास करते हैं। एन = 1 के लिए, हमारे पास आदर्श मिश्रण उपकरण के लिए एक स्पष्ट समाधान है।
आइए हम आलेखों में दिखाएं कि कैसे कोशिकाओं की संख्या में वृद्धि हमें एक आदर्श मिश्रण उपकरण से एक पूर्ण विस्थापन उपकरण में जाने के लिए सेल मॉडल का उपयोग करने की अनुमति दे सकती है।

एच  प्रवाह में अनुदैर्ध्य मिश्रण को बाहर करने के लिए, उपकरण की कार्यशील मात्रा को विभाजित किया जाता है।
प्रवाह में अनुदैर्ध्य मिश्रण को बाहर करने के लिए, उपकरण की कार्यशील मात्रा को विभाजित किया जाता है।
उपकरण कैस्केडिंग का भी उपयोग किया जाता है - रासायनिक प्रतिक्रियाओं के परिणामों को बराबर करने के लिए तकनीकी उपकरणों का एक सीरियल कनेक्शन।
रासायनिक प्रतिक्रियाओं के प्रवाह में कैनेटीक्स का मॉडलिंग, प्रवाह की विशेषताओं को ध्यान में रखते हुए, उपकरण की विशेषताओं (आउटपुट संरचना) की गणना करने की अनुमति देता है।
भौतिक रसायन विज्ञान विभाग
अब्रामेनकोव ए.वी.
काइनेट
कैनेटीक्स के संख्यात्मक अनुकरण के लिए कार्यक्रम
जटिल रासायनिक प्रतिक्रियाएं
KINET कार्यक्रम को प्रत्यक्ष और व्युत्क्रम गतिज समस्याओं को हल करने के लिए डिज़ाइन किया गया है। प्रारंभिक डेटा के रूप में, प्रक्रिया की गतिज योजना (तंत्र) को दर स्थिरांक के संकेत के साथ सरल प्रतिक्रियाओं के एक सेट के रूप में सेट किया जाता है, और प्रतिक्रिया समीकरणों को सामान्य रासायनिक संकेतन के करीब एक रूप में लिखा जा सकता है। इसके अलावा, प्रक्रिया की स्थिति इंगित की जाती है - अभिकर्मकों और तापमान की प्रारंभिक सांद्रता, साथ ही समय अंतराल जिस पर समाधान प्राप्त किया जाना है। व्युत्क्रम गतिज समस्या के मामले में, प्रयोगात्मक गतिज वक्रों को निर्दिष्ट करना भी आवश्यक है।
कार्यक्रम स्वतंत्र रूप से अंतर समीकरणों की एक प्रणाली बनाता है और इसे एकीकृत करता है। परिणाम संख्यात्मक और ग्राफिक रूप से प्रस्तुत किए जाते हैं और अन्य कार्यक्रमों में उपयोग के लिए निर्यात किए जा सकते हैं।
KINET कार्यक्रम के अनुप्रयोग के कुछ उदाहरण पुस्तक में दिए गए हैं: "भौतिक रसायन विज्ञान पर व्यावहारिक कार्य: काइनेटिक्स और कटैलिसीस। इलेक्ट्रोकैमिस्ट्री "(अब्रामेनकोव ए.वी., आयुव ई.पी., अत्यक्षेवा एल.एफ. एट अल। वी.वी. लुनिन और ई.पी. आयुव द्वारा संपादित)। मॉस्को: एड। केंद्र "अकादमी", 2012। खंड I.8, "जटिल प्रतिक्रियाओं के कैनेटीक्स का गणितीय मॉडलिंग", पीपी। 70-102. प्रोग्राम का उपयोग करने के लिए विस्तृत मार्गदर्शिका के लिए, UserGuide.pdf फ़ाइल देखें।
सिस्टम आवश्यकताएं:
- विंडोज एक्सपी / विस्टा / 7 (32-बिट या 64-बिट),
- प्रोग्राम फ़ाइलों को रखने के लिए डिस्क या फ्लैश ड्राइव पर 3.7 एमबी,
- स्क्रीन रिज़ॉल्यूशन कम से कम 1024 x 768 (अधिमानतः अधिक)।
स्थापाना निर्देश
KINET प्रोग्राम को स्थापित करने के लिए, डाउनलोड किए गए संग्रह (सबफ़ोल्डर की आंतरिक संरचना को ध्यान में रखते हुए) को "प्रोग्राम फ़ाइलें" फ़ोल्डर या किसी अन्य फ़ोल्डर में अनपैक करें और wkinet.exe निष्पादन योग्य फ़ाइल लॉन्च करने के लिए डेस्कटॉप पर एक शॉर्टकट बनाएं।
काइनेट फ़ोल्डर के अंदर, लोकेल सबफ़ोल्डर में प्रोग्राम इंटरफ़ेस का रूसी में अनुवाद होता है। इस सबफ़ोल्डर की अनुपस्थिति में, प्रोग्राम चालू रहेगा, लेकिन इसमें एक अंग्रेज़ी इंटरफ़ेस होगा।
उपयोगकर्ता प्रोफ़ाइल में डेटा संग्रहीत करने के लिए मानक फ़ोल्डर में kinet.ini फ़ाइल में अलग-अलग सेटिंग्स सहेजी जाती हैं। विंडोज़ के आधुनिक संस्करणों पर, यह आमतौर पर सी: \ उपयोगकर्ता \ फ़ोल्डर है<Имя пользователя>\ एप्लिकेशन डेटा \ काइनेट \
प्रोग्राम विंडोज रजिस्ट्री को कुछ भी नहीं लिखता है, इसलिए इसे कंप्यूटर से पूरी तरह से हटाने के लिए, प्रोग्राम फ़ाइलों के साथ मुख्य काइनेट फ़ोल्डर और उपयोगकर्ता प्रोफ़ाइल में काइनेट फ़ोल्डर को हटाने के लिए पर्याप्त है (ऊपर देखें)।
KINET कार्यक्रम स्वतंत्र रूप से वितरित किया जाता है (Kinet \ doc \ लाइसेंस_ru.txt फ़ाइल में लाइसेंस समझौता देखें)।
सिमुलेशन कदम
सैद्धांतिक और प्रायोगिक मॉडलिंग दोनों की प्रक्रिया में निम्नलिखित चरण होते हैं:
1. एक मॉडल का निर्माण।
2. मॉडल का अध्ययन करें।
3. एक्सट्रपलेशन - प्राप्त डेटा को मूल वस्तु के ज्ञान के क्षेत्र में स्थानांतरित करना।
पहले चरण में, वस्तु के प्रत्यक्ष अध्ययन की असंभवता या अक्षमता का एहसास होने पर, इसका मॉडल बनाया जाता है। इस चरण का उद्देश्य एक मध्यस्थ वस्तु द्वारा मूल के पूर्ण प्रतिस्थापन के लिए स्थितियां बनाना है जो इसके आवश्यक मापदंडों को पुन: पेश करता है।
दूसरे चरण में, मॉडल का अध्ययन स्वयं किया जाता है - एक विशिष्ट संज्ञानात्मक कार्य को हल करने के लिए जितना आवश्यक हो उतना विस्तृत। यहां, शोधकर्ता मॉडल के व्यवहार का निरीक्षण कर सकता है, उस पर प्रयोग कर सकता है, उसकी विशेषताओं को माप सकता है या उनका वर्णन कर सकता है - मॉडल की बारीकियों के आधार पर और प्रारंभिक संज्ञानात्मक कार्य पर। दूसरे चरण का उद्देश्य मॉडल के बारे में आवश्यक जानकारी प्राप्त करना है।
तीसरा चरण (एक्सट्रपलेशन) मूल वस्तु पर "वापसी" है, अर्थात। मॉडल के बारे में प्राप्त ज्ञान की व्याख्या, उनकी स्वीकार्यता का आकलन और, तदनुसार, मूल के लिए उनका आवेदन, अनुमति देता है, यदि सफल हो, तो मूल संज्ञानात्मक समस्या को हल करने के लिए।
ये चरण एक प्रकार का अनुकरण चक्र लागू करते हैं, जिसके दौरान मॉडल और मूल एक दूसरे से संबंधित होते हैं। (चित्र एक)।
चावल। 1. सिमुलेशन कदम
रसायन विज्ञान में सिमुलेशन
मॉडलिंग अणु, रासायनिक प्रक्रियाएं और प्रतिक्रियाएं
सामग्री (प्रायोगिक) मॉडलिंग का व्यापक रूप से रसायन विज्ञान में उपयोग किया जाता है ताकि पदार्थों की संरचना और रासायनिक प्रतिक्रियाओं के पाठ्यक्रम की विशेषताओं को समझने और अध्ययन करने के लिए, रासायनिक तकनीकी प्रक्रियाओं आदि के लिए इष्टतम स्थितियों की पहचान की जा सके।
जैव रसायन और औषध विज्ञान मेंमॉडलिंग एक बहुत ही महत्वपूर्ण भूमिका निभाता है। औषध विज्ञान की प्रगति नई, अधिक उन्नत दवाओं की निरंतर खोज और निर्माण की विशेषता है। हाल के वर्षों में, नई दवाएं बनाते समय, जैविक रूप से सक्रिय पदार्थ को आधार के रूप में नहीं लिया जाता है, जैसा कि पहले किया गया था, लेकिन सब्सट्रेट जिसके साथ यह इंटरैक्ट करता है (रिसेप्टर, एंजाइम, आदि)। इस तरह के अध्ययनों के लिए उन मैक्रोमोलेक्यूल्स की त्रि-आयामी संरचना पर सबसे विस्तृत डेटा की आवश्यकता होती है जो दवा के लिए मुख्य लक्ष्य हैं। वर्तमान में, इस तरह के डेटा का एक बैंक है, जिसमें महत्वपूर्ण संख्या में एंजाइम और न्यूक्लिक एसिड शामिल हैं। कई कारकों ने इस दिशा में प्रगति में योगदान दिया है। सबसे पहले, एक्स-रे संरचनात्मक विश्लेषण में सुधार किया गया था, और परमाणु चुंबकीय अनुनाद पर आधारित स्पेक्ट्रोस्कोपी विकसित की गई थी। बाद की विधि ने मौलिक रूप से नई संभावनाएं खोलीं, क्योंकि इससे समाधान में पदार्थों की त्रि-आयामी संरचना स्थापित करना संभव हो गया, यानी। एक गैर-क्रिस्टलीय अवस्था में। एक आवश्यक बात यह थी कि आनुवंशिक इंजीनियरिंग की सहायता से विस्तृत रासायनिक और भौतिक-रासायनिक अनुसंधान के लिए पर्याप्त संख्या में सब्सट्रेट प्राप्त करना संभव था।
कई मैक्रोमोलेक्यूल्स के गुणों पर उपलब्ध डेटा का उपयोग करके, कंप्यूटर का उपयोग करके उनकी संरचना का अनुकरण करना संभव है। यह न केवल पूरे अणु की ज्यामिति का एक स्पष्ट विचार देता है, बल्कि इसके सक्रिय केंद्रों का भी, जो लिगैंड्स के साथ बातचीत करते हैं। सब्सट्रेट सतह की स्थलाकृति की विशेषताएं, इसके संरचनात्मक तत्वों की प्रकृति और अंतर्जात पदार्थों या ज़ेनोबायोटिक्स के साथ संभावित प्रकार के अंतर-परमाणु बातचीत की जांच की जाती है। दूसरी ओर, अणुओं का कंप्यूटर मॉडलिंग, ग्राफिक सिस्टम और संबंधित सांख्यिकीय विधियों का उपयोग, आपको औषधीय पदार्थों की त्रि-आयामी संरचना और उनके इलेक्ट्रॉनिक क्षेत्रों के वितरण की पूरी तस्वीर प्राप्त करने की अनुमति देता है। शारीरिक रूप से सक्रिय पदार्थों और सब्सट्रेट के बारे में इस तरह की सारांश जानकारी उच्च पूरकता और आत्मीयता के साथ संभावित लिगैंड के कुशल निर्माण की सुविधा प्रदान करनी चाहिए। अभी तक ऐसे अवसर केवल सपने में ही देखे जा सकते थे - अब वे साकार हो रहे हैं।
अणुओं का कंप्यूटर मॉडलिंग कई अनुमानों और मान्यताओं पर आधारित है। इस प्रकार, यह माना जाता है कि अणुओं की ऊर्जा अंतरिक्ष में उनके परमाणुओं के निर्देशांक द्वारा ही निर्धारित होती है। लेकिन वास्तव में, अणु गतिहीन नहीं होते हैं, और कंप्यूटर पर ऊर्जा की गणना स्थिर अणुओं पर की जाती है। वर्तमान में, आणविक गतिकी के तरीके विकसित किए जा रहे हैं जो अणुओं की तापीय गति को ध्यान में रखते हैं, लेकिन अभी भी ऐसे कोई दृष्टिकोण नहीं हैं जो ऊर्जा के एन्ट्रापी घटक को मज़बूती से ध्यान में रखें। इसके अलावा, एक उचित समय सीमा के भीतर, कई पिकोसेकंड के क्रम में सिस्टम के जीवनकाल की गणना करना संभव है।
प्रोटीन की त्रि-आयामी संरचना का अध्ययन करना बड़ी कठिनाइयाँ प्रस्तुत करता है। आज तक, ऐसी कोई विधि नहीं है जो अमीनो एसिड अनुक्रम के आधार पर प्रोटीन की त्रि-आयामी संरचना का सटीक अनुमान लगा सके। यद्यपि उपमाओं की विधि का उपयोग किया जाता है, जब यह माना जाता है कि विभिन्न प्रोटीनों के समान अमीनो एसिड क्षेत्रों को एक समान तरीके से मोड़ा जाता है। त्रि-आयामी छवियों का प्रायोगिक अधिग्रहण कई कठिनाइयों से भरा है: एक्स-रे संरचनात्मक विश्लेषण के लिए, प्रोटीन क्रिस्टलीकरण की आवश्यकता होती है (जो केवल घुलनशील प्रोटीन के लिए संभव है), और परमाणु चुंबकीय अनुनाद की क्षमता प्रोटीन के आणविक आकार द्वारा सीमित है। .
आणविक जीव विज्ञान और जैव रसायन के क्षेत्र में मौलिक और अनुप्रयुक्त अनुसंधान दोनों के लिए आणविक मॉडलिंग की भूमिका लगातार बढ़ रही है। यह गणितीय तंत्र के सुधार, और कंप्यूटर प्रौद्योगिकी की उत्पादकता में वृद्धि, और बड़ी मात्रा में तथ्यात्मक सामग्री के संचय के साथ जुड़ा हुआ है जिसके लिए विश्लेषण की आवश्यकता होती है।
रासायनिक रिएक्टरों का अनुकरणइसका उपयोग किसी भी आकार के उपकरणों में दी गई शर्तों के तहत रासायनिक तकनीकी प्रक्रियाओं के परिणामों की भविष्यवाणी करने के लिए किया जाता है। भौतिक मॉडलिंग का उपयोग करके एक छोटे रिएक्टर से एक औद्योगिक रिएक्टर में बड़े पैमाने पर संक्रमण करने के प्रयास प्रक्रिया के रासायनिक और भौतिक घटकों की समानता के लिए शर्तों की असंगति के कारण असफल रहे (दर पर भौतिक कारकों का प्रभाव) विभिन्न आकारों के रिएक्टरों में रासायनिक रूपांतरण काफी भिन्न होता है)। इसलिए, बड़े पैमाने पर संक्रमण के लिए, अनुभवजन्य तरीकों का मुख्य रूप से उपयोग किया गया था: प्रक्रियाओं का अध्ययन क्रमिक रूप से बढ़ते रिएक्टरों (प्रयोगशाला, बढ़े हुए, पायलट, अर्ध-औद्योगिक स्थापना, औद्योगिक रिएक्टर) में किया गया था।
गणितीय मॉडलिंग ने पूरे रिएक्टर की जांच करने और बड़े पैमाने पर संक्रमण करने की अनुमति दी। एक रिएक्टर में प्रक्रिया में विभिन्न संरचनात्मक स्तरों पर बड़ी संख्या में रासायनिक और भौतिक अंतःक्रियाएं होती हैं - एक अणु, एक मैक्रो-क्षेत्र, एक रिएक्टर तत्व, एक रिएक्टर। प्रक्रिया के संरचनात्मक स्तरों के अनुसार, रिएक्टर का एक बहुस्तरीय गणितीय मॉडल बनाया गया है। पहला स्तर (रासायनिक परिवर्तन उचित) गतिज मॉडल से मेल खाता है, जिसके समीकरण प्रक्रिया की व्यावहारिक स्थितियों को कवर करते हुए, उनके परिवर्तनों की पूरी श्रृंखला में अभिकारकों, तापमान और दबाव की एकाग्रता पर प्रतिक्रिया दर की निर्भरता का वर्णन करते हैं। अगले संरचनात्मक स्तरों की प्रकृति रिएक्टर के प्रकार पर निर्भर करती है। उदाहरण के लिए, उत्प्रेरक के एक निश्चित बिस्तर वाले रिएक्टर के लिए, दूसरा स्तर एक प्रक्रिया है जो एक उत्प्रेरक अनाज पर होती है, जब एक छिद्रपूर्ण अनाज में पदार्थ स्थानांतरण और गर्मी हस्तांतरण आवश्यक होता है। प्रत्येक बाद के संरचनात्मक स्तर में पिछले सभी घटक भागों के रूप में शामिल होते हैं, उदाहरण के लिए, एक उत्प्रेरक अनाज पर प्रक्रिया के गणितीय विवरण में स्थानांतरण समीकरण और गतिज दोनों शामिल हैं। तीसरे स्तर के मॉडल में उत्प्रेरक बिस्तर, आदि में पदार्थ, गर्मी और गति के हस्तांतरण के लिए समीकरण भी शामिल हैं। अन्य प्रकार के रिएक्टरों के मॉडल (एक द्रवित बिस्तर के साथ, एक निलंबित उत्प्रेरक के साथ स्तंभ प्रकार, आदि) भी हैं। एक पदानुक्रमित संरचना।
गणितीय मॉडलिंग का उपयोग करते हुए, प्रक्रिया के लिए इष्टतम स्थितियों का चयन किया जाता है, उत्प्रेरक की आवश्यक मात्रा, रिएक्टर का आकार और आकार, प्रारंभिक और सीमा स्थितियों के लिए प्रक्रिया की पैरामीट्रिक संवेदनशीलता, क्षणिक मोड निर्धारित किए जाते हैं, और स्थिरता की स्थिरता प्रक्रिया की भी जांच की जा रही है। कई मामलों में, सैद्धांतिक अनुकूलन पहले किया जाता है - इष्टतम स्थितियां निर्धारित की जाती हैं जिसके तहत उपयोगी उत्पाद की उपज सबसे बड़ी होती है, भले ही उन्हें बाहर किया जा सके, और फिर, दूसरे चरण में, एक इंजीनियरिंग समाधान है चयनित है जो आर्थिक और अन्य संकेतकों को ध्यान में रखते हुए सैद्धांतिक इष्टतम मोड के लिए सर्वोत्तम दृष्टिकोण की अनुमति देता है। पाए गए मोड के कार्यान्वयन और रिएक्टर के सामान्य संचालन के लिए, रिएक्टर के क्रॉस सेक्शन पर प्रतिक्रिया मिश्रण का एक समान वितरण और संरचना और तापमान में भिन्न प्रवाह के मिश्रण की पूर्णता सुनिश्चित करना आवश्यक है। इन कार्यों को चयनित रिएक्टर डिजाइन के भौतिक (एयरोहाइड्रोडायनामिक) मॉडलिंग द्वारा हल किया जाता है।
विभिन्न प्रक्रियाओं का अध्ययन करने के लिए जिसमें चरण और रासायनिक परिवर्तन होते हैं, वे उपयोग करते हैं थर्मोडायनामिक मॉडलिंग के तरीके.
चरण-रासायनिक परिवर्तनों का थर्मोडायनामिक मॉडलिंग, एक तरफ, रासायनिक थर्मोडायनामिक्स के नियमों और विधियों पर, दूसरी ओर, अत्यधिक समस्याओं को हल करने के लिए गणितीय उपकरण पर आधारित है। इन दो दृष्टिकोणों का एक पूर्ण संयोजन एक गणना पद्धति को लागू करना संभव बनाता है जिसमें अध्ययन के तहत प्रणालियों की प्रकृति और घटक प्रकृति पर मौलिक प्रतिबंध नहीं हैं।
चरण और रासायनिक परिवर्तनों से जुड़ी विभिन्न व्यावहारिक और सैद्धांतिक समस्याओं का अध्ययन करने के लिए, प्रक्रिया के भौतिक-रासायनिक सार का गहन और विस्तृत अध्ययन आवश्यक है, चरण की नियमितता और इस प्रक्रिया में होने वाले रासायनिक परिवर्तनों की पहचान, राज्य के मापदंडों का प्रभाव (तापमान, दबाव, प्रतिक्रिया मिश्रण की संरचना, आदि)।
अधिकांश वास्तविक भौतिक रासायनिक प्रक्रियाओं की जटिलता वर्णित समस्याओं को विशेष रूप से प्रयोगात्मक रूप से हल करने की अनुमति नहीं देती है। संभावित दृष्टिकोणों का विश्लेषण आधुनिक सिद्धांतों और भौतिक-रासायनिक और गणितीय मॉडलिंग के तरीकों और थर्मोडायनामिक अभ्यावेदन का उपयोग करके गणना की प्रभावशीलता को दर्शाता है। इन विधियों का उपयोग करके, चरण और रासायनिक परिवर्तनों का विस्तृत अध्ययन किया जा सकता है।
सैद्धांतिक मॉडलिंग
रासायनिक विज्ञान के विकास में सैद्धांतिक मॉडलिंग की भूमिका विशेष रूप से महत्वपूर्ण है, क्योंकि परमाणुओं और अणुओं की दुनिया शोधकर्ता के प्रत्यक्ष अवलोकन से छिपी हुई है। इसलिए, अप्रत्यक्ष डेटा का उपयोग करके अदृश्य वस्तुओं के मॉडल बनाकर अनुभूति की जाती है।
चावल। 2. मॉडल बनाना और संशोधित करना
सैद्धांतिक मॉडलिंग की प्रक्रिया, जैसा कि ऊपर उल्लेख किया गया है, चरणों में किया जाता है: एक मॉडल का निर्माण, मॉडल का अध्ययन और एक्सट्रपलेशन। प्रत्येक चरण में, कुछ कार्यों की पहचान की जा सकती है जो इसके कार्यान्वयन के लिए आवश्यक हैं। (चित्र 2)।मॉडलों को पूरक बनाया जा सकता है, बदला जा सकता है और यहां तक कि नए मॉडलों द्वारा प्रतिस्थापित भी किया जा सकता है। ऐसी प्रक्रियाएं तब होती हैं जब शोधकर्ताओं को नए तथ्यों का सामना करना पड़ता है जो निर्मित मॉडल का खंडन करते हैं। नया मॉडल पुराने मॉडल और नए प्राप्त आंकड़ों के बीच अंतर्विरोधों पर पुनर्विचार का परिणाम है।
आइए सैद्धांतिक मॉडलिंग में अनुभूति प्रक्रिया की बारीकियों पर विचार करें।
आदर्श मॉडलिंग सैद्धांतिक ज्ञान के तरीकों में से एक है। इस प्रकार, सैद्धांतिक ज्ञान के ऐसे संरचनात्मक घटक जैसे समस्या, परिकल्पना और सिद्धांत को सैद्धांतिक मॉडलिंग का आधार बनाना चाहिए।
तथ्यात्मक सामग्री के संचय और उसके विश्लेषण के बाद, समस्या की पहचान की जाती है और उसे तैयार किया जाता है। समस्या सैद्धांतिक ज्ञान का एक रूप है, जिसकी सामग्री कुछ ऐसी है जिसे अभी तक मनुष्य द्वारा पहचाना नहीं गया है, लेकिन इसे पहचानने की आवश्यकता है। दूसरे शब्दों में, यह अज्ञान का ज्ञान है, एक प्रश्न जो अनुभूति के दौरान उत्पन्न हुआ और जिसके उत्तर की आवश्यकता है। समस्या ज्ञान का जमे हुए रूप नहीं है, बल्कि एक प्रक्रिया है जिसमें दो मुख्य बिंदु (ज्ञान की गति के चरण) शामिल हैं - इसका निर्माण और समाधान। पिछले तथ्यों और सामान्यीकरणों से समस्या ज्ञान की सही व्युत्पत्ति, समस्या को सही ढंग से प्रस्तुत करने की क्षमता इसके सफल समाधान के लिए एक आवश्यक शर्त है। "किसी समस्या को हल करना अक्सर उसे हल करने की तुलना में अधिक आवश्यक होता है, जो केवल गणितीय या प्रयोगात्मक कला का मामला हो सकता है। नए प्रश्न पूछना, नई संभावनाएं विकसित करना, पुरानी समस्याओं को एक नए कोण से देखना रचनात्मक कल्पना की आवश्यकता है और विज्ञान में वास्तविक सफलता को दर्शाता है। "
वी। हाइजेनबर्ग ने नोट किया कि वैज्ञानिक समस्याओं के निर्माण और समाधान के लिए निम्नलिखित की आवश्यकता होती है: क) अवधारणाओं की एक निश्चित प्रणाली जिसकी मदद से शोधकर्ता कुछ घटनाओं को रिकॉर्ड करेगा; बी) अध्ययन के उद्देश्यों और हल की जा रही समस्याओं की प्रकृति को ध्यान में रखते हुए चुने गए तरीकों की एक प्रणाली; ग) वैज्ञानिक परंपराओं पर निर्भरता, क्योंकि, हाइजेनबर्ग के अनुसार, "परंपरा, ऐतिहासिक विकास की प्रक्रिया एक समस्या को चुनने में एक आवश्यक भूमिका निभाती है," हालांकि, निश्चित रूप से, वैज्ञानिक के हित और झुकाव स्वयं एक निश्चित महत्व के हैं।
के. पॉपर के अनुसार, विज्ञान की शुरुआत टिप्पणियों से नहीं, बल्कि समस्याओं से होती है, और इसका विकास एक समस्या से दूसरी समस्या में - कम गहरे से गहरे तक संक्रमण है। उनकी राय में, समस्याएँ या तो एक अलग सिद्धांत में एक विरोधाभास के परिणाम के रूप में उत्पन्न होती हैं, या जब दो अलग-अलग सिद्धांत टकराते हैं, या सिद्धांत के अवलोकन के साथ टकराव के परिणामस्वरूप उत्पन्न होते हैं।
इस प्रकार, एक वैज्ञानिक समस्या एक विरोधाभासी स्थिति (विपरीत पदों के रूप में अभिनय) की उपस्थिति में व्यक्त की जाती है, जिसके लिए एक उपयुक्त समाधान की आवश्यकता होती है। समस्या को प्रस्तुत करने और हल करने के तरीके पर निर्णायक प्रभाव सबसे पहले, उस युग की सोच की प्रकृति है जिसमें समस्या तैयार की जाती है, और दूसरी बात, उन वस्तुओं के बारे में ज्ञान का स्तर जो समस्या उत्पन्न होती है। प्रत्येक ऐतिहासिक युग में समस्या स्थितियों के अपने विशिष्ट रूप होते हैं।
पहचानी गई समस्या को हल करने के लिए, वैज्ञानिक एक परिकल्पना तैयार करता है। एक परिकल्पना सैद्धांतिक ज्ञान का एक रूप है जिसमें कई तथ्यों के आधार पर एक धारणा तैयार की जाती है, जिसका सही मूल्य अनिश्चित होता है और इसे सिद्ध करने की आवश्यकता होती है। काल्पनिक ज्ञान संभावित है, विश्वसनीय नहीं है, और इसके लिए सत्यापन और औचित्य की आवश्यकता होती है। आगे रखी गई परिकल्पनाओं को सिद्ध करने के क्रम में, उनमें से कुछ एक सच्चे सिद्धांत बन जाते हैं, अन्य संशोधित, परिष्कृत और ठोस हो जाते हैं, अन्य को त्याग दिया जाता है, यदि परीक्षण नकारात्मक परिणाम देता है तो भ्रम में बदल जाते हैं। एक नई परिकल्पना का निर्माण, एक नियम के रूप में, पुराने के परीक्षण के परिणामों पर निर्भर करता है, भले ही ये परिणाम नकारात्मक हों।
इसलिए, उदाहरण के लिए, परीक्षण के बाद प्लैंक द्वारा सामने रखी गई क्वांटम परिकल्पना एक वैज्ञानिक सिद्धांत बन गई, और "कैलोरिक", "फ्लॉजिस्टन", "ईथर", आदि के अस्तित्व के बारे में परिकल्पनाओं को पुष्टि नहीं मिली, उनका खंडन किया गया, में चला गया। त्रुटि। परिकल्पना का चरण भी डी.आई. द्वारा पारित किया गया था। मेंडेलीव आवधिक कानून।
डि मेंडेलीव का मानना था कि घटनाओं के एक उद्देश्यपूर्ण, व्यवस्थित अध्ययन के संगठन में, कुछ भी परिकल्पना के निर्माण को प्रतिस्थापित नहीं कर सकता है। "वे," महान रूसी रसायनज्ञ ने लिखा, "विज्ञान के लिए और विशेष रूप से इसके अध्ययन के लिए आवश्यक हैं। वे सद्भाव और सादगी देते हैं, जो उनके प्रवेश के बिना हासिल करना मुश्किल है। किसी से भी सच होने का समय। "
मेंडेलीव के अनुसार, एक परिकल्पना प्राकृतिक विज्ञान ज्ञान का एक आवश्यक तत्व है, जिसमें आवश्यक रूप से शामिल हैं: क) तथ्यों का संग्रह, विवरण, व्यवस्थितकरण और अध्ययन; बी) घटना के कारण संबंध के बारे में एक परिकल्पना या धारणा तैयार करना; ग) परिकल्पनाओं के तार्किक परिणामों का प्रायोगिक सत्यापन; d) परिकल्पनाओं को विश्वसनीय सिद्धांतों में परिवर्तित करना या पहले से स्वीकृत परिकल्पना को त्यागना और एक नई परिकल्पना को सामने रखना। डि मेंडेलीव ने स्पष्ट रूप से समझा कि एक परिकल्पना के बिना कोई विश्वसनीय सिद्धांत नहीं हो सकता है: "दृश्य और प्रत्यक्ष अवलोकन के अधीन अवलोकन, चित्रण और वर्णन - इंद्रियों की सहायता से, हम अध्ययन के दौरान आशा कर सकते हैं कि पहले परिकल्पनाएं दिखाई देंगी, और फिर सिद्धांत जो अध्ययन किया जा रहा है उसके आधार पर अब क्या आवश्यक है।"
इस प्रकार, एक परिकल्पना तभी तक अस्तित्व में रह सकती है जब तक कि वह अनुभव के विश्वसनीय तथ्यों का खंडन न करे, अन्यथा वह केवल एक कल्पना बन जाती है। यह सत्य के चरित्र को प्राप्त करते हुए, संबंधित प्रयोगात्मक तथ्यों (विशेषकर प्रयोग द्वारा) द्वारा सत्यापित (सत्यापित) किया जाता है। एक परिकल्पना फलदायी होती है यदि यह नए ज्ञान और अनुभूति के नए तरीकों को जन्म दे सकती है, जिससे कि घटनाओं की एक विस्तृत श्रृंखला की व्याख्या की जा सके।
इसके अनुप्रयोग में वैज्ञानिक और सैद्धांतिक ज्ञान के विकास की एक विधि के रूप में परिकल्पना निम्नलिखित मुख्य चरणों से गुजरती है।
1. विज्ञान में पहले से मौजूद ज्ञात तथ्यों और कानूनों और सिद्धांतों के आधार पर अध्ययन के तहत घटना की व्याख्या करने का प्रयास। यदि यह प्रयास विफल रहता है, तो एक और कदम उठाया जाता है।
2. इस घटना के कारणों और पैटर्न, इसके गुणों, कनेक्शन और संबंधों, इसकी उत्पत्ति और विकास आदि के बारे में अनुमान लगाना, अनुमान लगाना। अनुभूति के इस स्तर पर, सामने रखी गई स्थिति एक संभावित ज्ञान है जो अभी तक तार्किक रूप से सिद्ध नहीं हुआ है और अनुभव से इतना पुष्ट नहीं है कि इसे विश्वसनीय माना जाए। अक्सर, एक ही घटना की व्याख्या करने के लिए कई धारणाएँ सामने रखी जाती हैं।
3. परिकल्पना की वैधता के लिए उपरोक्त शर्तों के आधार पर ठोसता का मूल्यांकन, मान्यताओं की प्रभावशीलता और उनके सबसे संभावित सेट से चयन।
4. ज्ञान की एक अभिन्न प्रणाली में आगे की धारणा की तैनाती और उनके बाद के अनुभवजन्य सत्यापन के उद्देश्य से इसके परिणामों की कटौतीत्मक व्युत्पत्ति।
5. परिकल्पना से सामने रखे गए परिणामों का प्रायोगिक, प्रायोगिक सत्यापन। इस परीक्षण के परिणामस्वरूप, परिकल्पना या तो एक वैज्ञानिक सिद्धांत के "श्रेणी में गुजरती है", या इसका खंडन किया जाता है, "वैज्ञानिक दृश्य छोड़ देता है।" हालांकि, यह ध्यान में रखा जाना चाहिए कि एक परिकल्पना के परिणामों की अनुभवजन्य पुष्टि पूरी तरह से इसकी सच्चाई की गारंटी नहीं देती है, और परिणामों में से एक का खंडन पूरी तरह से इसकी झूठी गवाही नहीं देता है। यह स्थिति विशेष रूप से वैज्ञानिक क्रांतियों की विशेषता है, जब मौलिक अवधारणाएं और विधियां मौलिक रूप से बाधित होती हैं और मौलिक रूप से नए विचार सामने आते हैं।
इस प्रकार, एक परिकल्पना के सत्य की निर्णायक परीक्षा अंततः अपने सभी रूपों में अभ्यास है, लेकिन सत्य की तार्किक (सैद्धांतिक) कसौटी भी काल्पनिक ज्ञान को साबित करने या खंडन करने में एक निश्चित (सहायक) भूमिका निभाती है। एक परीक्षण और सिद्ध परिकल्पना एक विश्वसनीय सत्य बन जाती है, यह एक वैज्ञानिक सिद्धांत बन जाती है।
जटिल प्रतिक्रियाओं के गतिज मॉडल के निर्माण के लिए विभिन्न रणनीतियाँ
रासायनिक कैनेटीक्स रासायनिक प्रतिक्रियाओं की दरों का विज्ञान है, रासायनिक संतुलन के रास्ते पर एक प्रतिक्रिया प्रणाली के गतिशील व्यवहार का। भौतिक रसायन विज्ञान का यह क्षेत्र रासायनिक प्रतिक्रियाओं के तंत्र के अध्ययन से निकटता से संबंधित है, क्योंकि रासायनिक गतिकी तंत्र का अध्ययन करने के तरीकों में से एक है, और प्रतिक्रिया तंत्र, जैसा कि अब स्पष्ट हो गया है, एक के निर्माण का आधार है पर्याप्त गतिज मॉडल।
20वीं शताब्दी, रासायनिक कैनेटीक्स के विजयी विकास की शताब्दी, समाप्त हो गई है, जिसमें प्राथमिक अधिनियम के सूक्ष्म स्तर और तंत्र की अभूतपूर्व जटिलता की विशेषता वाले बहुस्तरीय प्रक्रियाओं के मैक्रोलेवल दोनों शामिल हैं। एक विज्ञान के रूप में रासायनिक गतिकी की नींव नोबेल पुरस्कार विजेताओं जे. वैंट-हॉफ (1901), एस. अरहेनियस (1903), वी. ओस्टवाल्ड (1909) और एम. बोडेनस्टीन के कार्यों द्वारा सदी की शुरुआत में रखी गई थी। . प्राथमिक अधिनियम के सिद्धांत के विभिन्न पहलुओं को जी। आइरिंग, एम। पोल्यानी, वी। जी। लेविच और आर। आर। डोगोनाडज़े, नोबेल पुरस्कार विजेता के। फुकुई और आर। हॉफमैन (1981), जी। ताउबे (1983), आर। मार्कस द्वारा विकसित किया गया था। 1992) और कई अन्य शोधकर्ता। चेन रिएक्शन का सिद्धांत एम। बोडेनस्टीन, जे। क्रिस्टियनसेन और नोबेल पुरस्कार विजेता एन.एन.सेमेनोव और एस.एन. हिंशेलवुड (1956), उनके छात्रों और अनुयायियों के कार्यों द्वारा बनाया गया था।
नोबेल पुरस्कार तेजी से प्राथमिक प्रतिक्रियाओं (एम। ईजेन, जे। पोर्टर, आर। नॉरिश, 1967) के अध्ययन के तरीकों और परिणामों के साथ-साथ गैस-चरण प्रतिक्रियाओं के प्राथमिक कृत्यों की गतिशीलता का अध्ययन करने के तरीकों के विकास के लिए प्रदान किए गए थे। डी. हर्शबैक, जे. ली, जे. पोलानी, 1986)।
सजातीय और विषम उत्प्रेरक प्रतिक्रियाओं के कैनेटीक्स के क्षेत्र में उत्कृष्ट परिणाम प्राप्त हुए हैं। हम केवल सिद्धांत का उल्लेख करते हैं
अमानवीय सतहों पर विषम प्रतिक्रियाओं के कैनेटीक्स (एमआई टेमकिन और एसजेड रोजिंस्की), होरियुटी-टेमकिन की स्थिर प्रतिक्रियाओं के कैनेटीक्स का सिद्धांत, ओलेफिन के ऑक्सीडेटिव परिवर्तनों के पैलेडियम परिसरों द्वारा कटैलिसीस की खोज (आई मोइसेव, एम। एन। वर्गाफटिक, हां। Syrkin, Y.Smidt और अन्य) और विस्तृत गतिज अध्ययन (AP Karpinsky Prize, 1999) के आधार पर IIMoiseev द्वारा इन प्रक्रियाओं के सिद्धांत का निर्माण।
बीसवीं शताब्दी को प्राथमिक अधिनियम के भौतिक रसायन विज्ञान के एक नए क्षेत्र की उल्लेखनीय खोज के साथ ताज पहनाया गया, जिसे "फेमटोकेमिस्ट्री" कहा जाता है, और अमेरिकी वैज्ञानिक, मिस्र के ए। ज़ेवेल को रसायन विज्ञान में 1999 का नोबेल पुरस्कार "संक्रमण राज्यों के उनके अध्ययन के लिए" द्वारा ताज पहनाया गया था। फेमटोसेकंड विधि (10-15 सेकंड) लेजर स्पेक्ट्रोस्कोपी "। रासायनिक प्रतिक्रियाओं की दरों को मापने की सीमा तक पहुँच गया है। एक रासायनिक बंधन में परमाणुओं के एक कंपन के दौरान होने वाली प्रक्रियाओं का पालन करना संभव हो गया - 10 - 100 एफएस। एक पूर्ण वर्णक्रमीय चित्र के साथ प्रतिक्रिया समन्वय के साथ कई प्रतिक्रियाओं की संक्रमण स्थिति 0.1 के संकल्प के साथ दर्ज की जाती है। पड़ोसी ऊर्जा राज्यों के संकल्प का स्तर ~ 10 –4 सेमी -1 तक पहुंच गया है।
माइक्रोलेवल पर रासायनिक प्रतिक्रियाओं के "नोइक्विलिब्रियम" कैनेटीक्स के अध्ययन के सभी परिणाम रासायनिक कैनेटीक्स के मूल सिद्धांतों को प्रमाणित करने के लिए अत्यंत महत्वपूर्ण हैं, लेकिन अभी तक वे मैक्रोलेवल पर समस्याओं को हल करने के लिए बहुत कम उपयोग करते हैं - जटिल प्रतिक्रियाओं के तंत्र की जांच में मैक्सवेल-बोल्ट्ज़मैन वितरण की शर्तों के तहत गैसों, समाधानों और एक ठोस की सतह पर, अर्थात। रासायनिक प्रतिक्रियाओं के "संतुलन" कैनेटीक्स की समस्याएं। यदि गैस-चरण कट्टरपंथी-श्रृंखला प्रतिक्रियाओं के "संतुलन" कैनेटीक्स के लिए जटिल प्रतिक्रियाओं के तंत्र को स्पष्ट करने और गतिज मॉडल के निर्माण की समस्या व्यावहारिक रूप से हल हो गई है (प्राथमिक चरणों के ज्ञात दर स्थिरांक के साथ अधिकतम तंत्र या प्रतिक्रिया नेटवर्क के निर्माण की संभावना के कारण) ), तो समाधान और सतह पर जटिल बहु-मार्ग प्रक्रियाओं के लिए, यह कार्य अभी शुरुआत है। यह XXI सदी की समस्या है।
जटिल प्रक्रियाओं के तीन प्रकार के गणितीय मॉडल (गणितीय विवरण) हैं। स्टोकेस्टिक मॉडल अनुसंधान वस्तु में प्रक्रियाओं के संभाव्य प्रतिनिधित्व का उपयोग करते हैं। संभाव्यता वितरण कार्यों की गणना मॉडल के चर मापदंडों (रासायनिक प्रक्रियाओं के मामले में एकाग्रता, तापमान) के लिए की जाती है। ये मॉडल अभी भी शायद ही कभी रासायनिक कैनेटीक्स में उपयोग किए जाते हैं, लेकिन वे बड़े सिस्टम (रासायनिक परिसरों, रासायनिक पौधों) के व्यवहार का वर्णन और मॉडलिंग के लिए उपयोगी साबित हुए हैं। एक कार्यशील शोध वस्तु पर एक प्रयोग का वर्णन करने के लिए सांख्यिकीय मॉडल का उपयोग किया जाता है। प्रणाली में प्रवेश करने वाले चरों के मूल्यों और वस्तु में होने वाली प्रक्रियाओं (ब्लैक बॉक्स मॉडल) के बारे में भौतिक-रासायनिक जानकारी का उपयोग किए बिना सिस्टम छोड़ने वालों के बीच संबंध का वर्णन किया गया है। एक प्रणाली के व्यवहार का गणितीय विवरण आमतौर पर बहुपद के रूप में समीकरण होता है। मॉडल मापदंडों की सांख्यिकीय स्वतंत्रता सुनिश्चित करने के लिए, प्रयोग योजना का उपयोग किया जाता है (उदाहरण के लिए, ऑर्थोगोनल प्रयोगात्मक डिजाइन)। नियतात्मक मॉडल मॉडल की एक निश्चित संरचना के साथ भौतिक और रासायनिक प्रक्रियाओं के नियमों पर आधारित होते हैं। सैद्धांतिक रूप से आधारित गतिज मॉडल ऐसे ही मॉडल हैं। रासायनिक प्रक्रियाओं के नियतात्मक, संरचनात्मक, सैद्धांतिक रूप से प्रमाणित गतिज मॉडल (केएम) व्याख्यान के इस पाठ्यक्रम का विषय होंगे।
उत्प्रेरक प्रक्रिया के गणितीय मॉडलिंग में गणितीय मॉडलों का एक निश्चित पदानुक्रम होता है। पहले स्तर के मॉडल एक ठोस उत्प्रेरक के दाने पर या एक सजातीय प्रतिक्रिया में एक तरल चरण के प्राथमिक मात्रा में प्रक्रियाओं के गतिज मॉडल होते हैं, जो द्रव्यमान, गर्मी हस्तांतरण और हाइड्रोडायनामिक कारकों की प्रक्रियाओं से जटिल होते हैं। विषम कटैलिसीस में दूसरे स्तर के मॉडल उत्प्रेरक बिस्तर में प्रक्रियाओं पर विचार करते हैं, और सजातीय और विषम कटैलिसीस में तीसरे स्तर के मॉडल पूरे रिएक्टर के मॉडल हैं, जिसमें सभी हस्तांतरण प्रक्रियाएं और प्रवाह संरचना शामिल हैं। व्याख्यान के इस पाठ्यक्रम में प्रथम स्तर के मॉडल (सीएम) पर चर्चा की जाएगी। स्वचालित प्रक्रिया नियंत्रण प्रणाली बनाने के लिए, औद्योगिक रिएक्टरों (रिएक्टर के गणितीय मॉडल के घटकों के रूप में) की गणना करने के लिए, उत्प्रेरक प्रक्रियाओं को अनुकूलित करने के लिए, नई प्रतिक्रियाओं का अध्ययन करने के लिए ऐसे मॉडलों की आवश्यकता होती है।
"प्रतिक्रिया तंत्र" की अवधारणा के बारे में
तो, सीएम का निर्माण प्रक्रिया के तंत्र पर आधारित है, अर्थात। प्रारंभिक अवस्थाओं का एक समूह जो प्रारंभिक अभिकर्मकों को प्रतिक्रियाओं के अंतिम उत्पादों में बदल देता है, और उसी प्रतिक्रिया (उत्प्रेरक या गैर-उत्प्रेरक) के लिए ज्ञान और प्रतिमान की मौजूदा मात्रा द्वारा निर्धारित तंत्र का एक सीमित सेट होता है। रसायन विज्ञान।
उदाहरण के लिए, सुगंधित नाभिक ArX (गैर-उत्प्रेरक, धातु परिसरों द्वारा उत्प्रेरित या ArX से ArX तक इलेक्ट्रॉनों के स्थानांतरण से प्रेरित) में न्यूक्लियोफिलिक प्रतिस्थापन की प्रतिक्रिया के लिए, 8 तंत्र स्थापित किए गए हैं:



धातु उत्प्रेरक पर एक साधारण एथिलीन हाइड्रोजनीकरण प्रतिक्रिया के तेरह एकल-पथ और 80 दो-पथ तंत्र प्रस्तावित किए गए हैं। दूसरे शब्दों में, प्रत्येक प्रतिक्रिया प्रणाली (अभिकर्मकों, उत्प्रेरक) के लिए कई प्रारंभिक चरण होते हैं - एक प्रतिक्रिया नेटवर्क (अधिकतम तंत्र), जिनमें से अलग-अलग ब्लॉक उत्प्रेरक की प्रकृति, परिस्थितियों, सब्सट्रेट में प्रतिस्थापन के आधार पर कार्यान्वित किए जाते हैं। , और धातु उत्प्रेरक की ऑक्सीकरण अवस्था।
सदी के अंत में, तंत्र के अध्ययन के लिए भौतिक-रासायनिक और औपचारिक गतिज दृष्टिकोणों के संयोजन की रूपरेखा तैयार की गई थी। इस अवधारणा के दो घटकों की एकता के रूप में तंत्र पर एक दृष्टिकोण तैयार किया गया था - टोपोलॉजिकल (संरचनात्मक) और रासायनिक घटक, और उनकी समानता - तंत्र की संरचना (प्राथमिक चरणों के संबंध) को स्पष्ट रूप से स्थापित करना असंभव है। केवल एक औपचारिक गतिज विवरण के आधार पर, तथाकथित "तंत्र योजना", और फिर इसे रासायनिक सामग्री से भरें। सामान्य स्थिति में, इस तंत्र को निर्दिष्ट किए बिना और औपचारिक गतिज पद्धति के लिए उपयुक्त कार्यों को निर्धारित किए बिना, गतिज प्रयोगों से तंत्र योजना की सही पहचान के लिए आवश्यक जानकारी प्राप्त करना असंभव है।
इन सभी परिस्थितियों ने सीएम के निर्माण की पारंपरिक रणनीति को संशोधित करने की आवश्यकता पैदा की है।
मुख्यमंत्री के निर्माण के लिए वैकल्पिक रणनीतियाँ
सीएम के निर्माण की पारंपरिक प्रक्रिया में निम्नलिखित चरण शामिल हैं:
इस प्रक्रिया (रणनीति) का मुख्य नुकसान सभी चरणों के स्पष्ट निष्पादन के लिए एल्गोरिदम की कमी है। चूंकि प्रयोग को बड़ी संख्या में गणितीय मॉडल (समीकरण) द्वारा पर्याप्त रूप से वर्णित किया जा सकता है, शोधकर्ता के पास तंत्र की योजना (तंत्र की संरचना के बारे में) या प्रस्तावित समीकरणों के रूप के बारे में किसी प्रकार की परिकल्पना होनी चाहिए। इस मामले में, प्रयोग किए जाने के बाद संभावित परिकल्पनाओं (कभी-कभी सहज) का चयन होता है। गणितीय मॉडल से भौतिक मॉडल (विशेषकर बहु-मार्ग प्रतिक्रियाओं के लिए) (चरण (बी)) में संक्रमण के लिए कोई एल्गोरिदम नहीं है। प्रतिक्रिया तंत्र (चरण (सी)) में संक्रमण भी मनमाना है और औपचारिक नहीं है। इस रणनीति के सभी चरणों में, कम से कम एक समीकरण (और एक "तंत्र आरेख") प्राप्त करने की एक स्वाभाविक प्रवृत्ति होती है जो प्रयोग का खंडन नहीं करती है, और, अक्सर, अनुमानों के एक सेट के किसी भी भेदभाव का कोई सवाल ही नहीं है। . इसके विपरीत, तंत्र की ऐसी योजना के लेखक उस तंत्र को साबित करने के लिए प्रयोग करना शुरू करते हैं जो लेखक को सबसे उचित लगता है। साथ ही, यह लंबे समय से स्थापित किया गया है कि किसी भी परिकल्पना को साबित करना असंभव है। आप गैर-कार्यात्मक परिकल्पनाओं को निर्णायक रूप से त्याग सकते हैं और शेष परिकल्पनाओं के प्रयोग के साथ सहमति दिखा सकते हैं - कार्यशील परिकल्पनाओं का एक सेट। परिकल्पनाओं के एक सेट को सामने रखने और काम करने वाली परिकल्पनाओं के एक सेट को प्राप्त करने की समीचीनता को अमेरिकी भूविज्ञानी टी। चेम्बरलेन द्वारा 100 साल से भी अधिक समय पहले प्रमाणित किया गया था।
इस प्रकार, एक सीएम के निर्माण के लिए एक तर्कसंगत रणनीति कंप्यूटर और प्रभावी सॉफ्टवेयर की क्षमताओं द्वारा समर्थित एक स्पष्ट पद्धति से प्रमाणित काल्पनिक-निगमनात्मक तार्किक अनुसंधान योजना है। इस रणनीति का सार इसके चरणों के क्रम में परिलक्षित होता है:

परिकल्पना के भेदभाव में चरणों का भेदभाव, चरणों के ब्लॉक, व्यक्तिगत तंत्र, बहु-पथ प्रतिक्रियाओं में जंक्शन शामिल हो सकते हैं।
सीएम का प्रकार (गणितीय विवरण का रूप) तंत्र की विशेषताओं (रैखिक या अरेखीय), प्रक्रिया की स्थितियों (स्थिर, अर्ध-स्थिर, गैर-स्थिर), रिएक्टर के प्रकार (खुले, बंद) और पर निर्भर करता है। कई स्वीकृत धारणाएँ। एक रेखीय तंत्र एक ऐसा तंत्र है जिसके आगे और पीछे की दिशाओं में प्रारंभिक चरण मध्यवर्ती में रैखिक होते हैं - प्रारंभिक चरण में तीर के बाईं (या दाईं ओर) केवल एक मध्यवर्ती यौगिक स्थित होता है। यदि एक से अधिक मध्यवर्ती एक चरण (एक मध्यवर्ती के 2 अणुओं सहित) में भाग लेते हैं, तो चरण अरेखीय होते हैं और तंत्र अरेखीय होता है।
सीएम का सबसे आम प्रकार अंतर समीकरणों, बीजीय-अंतर या बीजीय समीकरणों की प्रणाली है
![]() , (1)
, (1)
जिसका दाहिना हाथ हमेशा प्राथमिक चरणों के वेग के कॉलम वेक्टर द्वारा तंत्र के चरणों (ट्रांसपोज़्ड) के लिए स्टोइकोमेट्रिक गुणांक के मैट्रिक्स का उत्पाद होता है ( ![]() ) स्थिर या अर्ध-स्थिर स्थितियों में प्रतिक्रिया के लिए रैखिक तंत्र के मामले में, समीकरण (1) के दाहिने हाथ को अभिकारकों (आर i) या मार्गों के लिए दरों (आर पी) की दरों के लिए आंशिक-तर्कसंगत समीकरणों में बदल दिया जाता है। . सामान्य स्थिति में, गैर-रेखीय तंत्र के लिए बीजीय समीकरणों की प्रणाली हल नहीं होती है, और प्रकार (1) के समीकरणों को सरल भिन्नात्मक तर्कसंगत रूप में कम नहीं किया जाता है।
) स्थिर या अर्ध-स्थिर स्थितियों में प्रतिक्रिया के लिए रैखिक तंत्र के मामले में, समीकरण (1) के दाहिने हाथ को अभिकारकों (आर i) या मार्गों के लिए दरों (आर पी) की दरों के लिए आंशिक-तर्कसंगत समीकरणों में बदल दिया जाता है। . सामान्य स्थिति में, गैर-रेखीय तंत्र के लिए बीजीय समीकरणों की प्रणाली हल नहीं होती है, और प्रकार (1) के समीकरणों को सरल भिन्नात्मक तर्कसंगत रूप में कम नहीं किया जाता है।
स्थिर परिस्थितियों में अमानवीय सतहों पर कैनेटीक्स के मामले में, वेग को प्रकार (2) (अमोनिया के संश्लेषण के लिए एम.आई. टेमकिन के समीकरण) के एक शक्ति समीकरण द्वारा भी वर्णित किया जा सकता है:
 (2)
(2)
गुणांक m = 0.5 लोहे के उत्प्रेरक के मामले में, k + / k - = K प्रतिक्रिया का संतुलन स्थिरांक है
विभिन्न मामलों के लिए गतिज मॉडल की विशेषताएं, गतिज समीकरणों को प्राप्त करने के तरीके और तर्कसंगत रणनीति के ढांचे में सीएम के निर्माण के तरीकों पर पाठ्यक्रम के बाद के खंडों में विचार किया जाएगा। पारंपरिक रणनीति में महारत हासिल करना होमवर्क (कोर्सवर्क) का विषय है।
आत्म-नियंत्रण के लिए प्रश्न
1) पारंपरिक रणनीति के नुकसान की सूची बनाएं।
2) एक तर्कसंगत रणनीति की पद्धतिगत पुष्टि।
3) एक तर्कसंगत रणनीति के मुख्य चरणों का नाम दें और केएम के निर्माण के सभी चरणों में इस रणनीति के लाभों की सूची बनाएं।
4) रैखिक और अरेखीय तंत्र के मामले में सीएम की विशेषताओं का नाम दें।
विषय के गहन अध्ययन के लिए साहित्य
1. श्मिट आर।, सपुनोव वीएन, अनौपचारिक कैनेटीक्स, एम।, मीर, 1985, 263 पी। (पारंपरिक रणनीति)।
2. ब्रुक एलजी, ज़िगार्निक एवी, टेमकिन ऑन, वैलेड्स-पेरेज़ आर।, प्रतिक्रियाओं के तंत्र के बारे में परिकल्पना के तरीके। पाठ्यपुस्तक, मास्को: MITHT, 1999।
3. Temkin ON, Brook LG, Zeigarnik AV, जटिल प्रतिक्रियाओं के तंत्र के अध्ययन और गतिज मॉडल के निर्माण के लिए रणनीति के कुछ पहलू, काइनेटिक्स और कटैलिसीस, 1993, खंड 34, संख्या 3, पी। 445 - 462।
4. टेमकिन ऑन, जटिल प्रतिक्रियाओं के कैनेटीक्स की समस्याएं, रॉस। केमिकल जर्नल, 2000, वी. 44, नंबर 4, पी. 58 - 65.




और बेसिक ऑर्गेनिक सिंथेसिस के रसायन विज्ञान और प्रौद्योगिकी विभाग के उत्प्रेरण, MITHT के नाम पर रखा गया एमवी लोमोनोसोव। पैलेडियम परिसरों के समाधान में प्रतिक्रिया (6) द्वारा ऐक्रेलिक एसिड संश्लेषण के तंत्र के बारे में परिकल्पना को सामने रखने के लिए, 11 परिवर्तनों का उपयोग किया गया: 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 11. का उपयोग करना केमनेट कार्यक्रम, हमने एक प्रतिक्रिया प्राप्त की। ..
एक उपाय, सोच की एक सहक्रियात्मक शैली वैज्ञानिकों, विचारकों, कलाकारों के बीच एक खुले रचनात्मक संवाद के लिए एक तरह का मंच हो सकता है, जिनके पास दुनिया के विभिन्न रचनात्मक दृष्टिकोण और विचार हैं। 2. सहक्रिया विज्ञान के कुछ विरोधाभासी परिणाम सहक्रिया विज्ञान में बहुत से नए विरोधाभासी विचार, चित्र और निरूपण उत्पन्न होते हैं। इसके अलावा, तालमेल की दृष्टि से, यह हो सकता है ...





...; वीसीएच3ओएच = 10 मिली; 0: 0: 0 = 5: 3: 2। आगे के शोध के दौरान इस प्रभाव के कारणों की जांच की जाएगी। 5. पेटेंट खोज 5.1। परिचय यह थीसिस पैलेडियम उत्प्रेरक की उपस्थिति में अल्काइन्स के ऑक्सीडेटिव कार्बोनिलेशन के दौरान कंपन शासन की घटना के लिए स्थितियों के अध्ययन के लिए समर्पित है। यह प्रक्रिया बहुत रुचि की है, क्योंकि यह आगे अनुमति देगी ...





प्रतिस्पर्धी माहौल में जीवित रहने और बाजार को सफलतापूर्वक विकसित करने के लिए, एक उद्यम को लंबी अवधि और वर्तमान अवधि के लिए स्पष्ट रूप से विकसित योजना की आवश्यकता होती है। अध्याय 2. ऑटोसर्विस सेवाओं के बाजार पर "एवीटीओडीओएम-एटीएक्स" एलएलसी के उद्यम की स्थिति का विश्लेषण 2.1 उद्यम की संक्षिप्त तकनीकी और आर्थिक विशेषताओं उद्यम "एव्टोडॉम-एटेक्स" की स्थापना प्रतिभागियों के निर्णय के आधार पर की गई थी। 23 ...
भौतिक रसायन विज्ञान में, रासायनिक प्रतिक्रिया की दर समीकरण के अनुसार निर्धारित की जाती है:
कहां डीक्यू- अभिकारक के द्रव्यमान में परिवर्तन, मोल।
डीटी- समय वृद्धि, एस।
वीप्रतिक्रिया स्थान का एक उपाय है।
सजातीय रासायनिक प्रतिक्रियाओं के बीच अंतर करें जिसमें शामिल सभी पदार्थ एक ही चरण (गैस या तरल) के भीतर हों। ऐसी प्रतिक्रियाओं के लिए, प्रतिक्रिया स्थान का माप मात्रा है, और वेग का आयाम होगा:।
विभिन्न चरणों (गैस-ठोस, गैस-तरल, तरल-तरल, ठोस-तरल) में पदार्थों के बीच विषम रासायनिक प्रतिक्रियाएं होती हैं। इस मामले में, वास्तविक रासायनिक प्रतिक्रिया इंटरफ़ेस पर महसूस की जाती है, जो प्रतिक्रिया स्थान का एक उपाय है।
विषम प्रतिक्रियाओं के लिए, दर का आयाम अलग है:।
प्रतिक्रियाशील पदार्थों के द्रव्यमान में परिवर्तन का अपना संकेत होता है। प्रारंभिक पदार्थों के लिए, प्रतिक्रिया के दौरान द्रव्यमान कम हो जाता है, द्रव्यमान में परिवर्तन का नकारात्मक संकेत होता है, और वेग का परिमाण ऋणात्मक मान लेता है। रासायनिक प्रतिक्रिया के उत्पादों के लिए, द्रव्यमान बढ़ता है, द्रव्यमान में परिवर्तन सकारात्मक होता है, और वेग का संकेत भी सकारात्मक माना जाता है।
एक साधारण रासायनिक प्रतिक्रिया पर विचार करें
सरल प्रतिक्रियाओं में वे शामिल हैं जो एक चरण में किए जाते हैं और अंत तक जाते हैं, अर्थात। अपरिवर्तनीय हैं।
आइए ऐसी रासायनिक प्रतिक्रिया की दर निर्धारित करें। इसके लिए सबसे पहले यह तय करना आवश्यक है कि किन पदार्थों की प्रतिक्रिया दर निर्धारित की जाएगी: आखिरकार, ए और बी प्रारंभिक पदार्थ हैं, और उनके द्रव्यमान में परिवर्तन नकारात्मक है, और सी अंतिम उत्पाद है, और इसका द्रव्यमान समय के साथ बढ़ता जाता है। इसके अलावा, प्रतिक्रिया में सभी स्टोइकोमेट्रिक गुणांक एकता के बराबर नहीं होते हैं, जिसका अर्थ है कि यदि प्रवाह दर ए कुछ समय के लिए 1 मोल के बराबर है, तो उसी समय के दौरान प्रवाह दर बी 2 मोल होगी, और, तदनुसार, A और B के द्रव्यमान में परिवर्तन से परिकलित दर मान आधे से भिन्न होंगे।
एक साधारण रासायनिक प्रतिक्रिया के लिए, दर का एक ही उपाय प्रस्तावित किया जा सकता है, जिसे निम्नानुसार निर्धारित किया जाता है:
कहां मैं- प्रतिक्रिया के i-वें प्रतिभागी की गति
एस आईप्रतिक्रिया में i-वें प्रतिभागी का स्टोइकोमेट्रिक गुणांक है।
प्रारंभिक पदार्थों के लिए स्टोइकोमेट्रिक गुणांक को सकारात्मक माना जाता है, प्रतिक्रिया उत्पादों के लिए वे नकारात्मक होते हैं।
यदि प्रतिक्रियाएं एक अलग प्रणाली में होती हैं जो बाहरी वातावरण के साथ पदार्थ का आदान-प्रदान नहीं करती है, तो केवल एक रासायनिक प्रतिक्रिया से सिस्टम में पदार्थ के द्रव्यमान में परिवर्तन होता है, और इसके परिणामस्वरूप, उनकी सांद्रता में। ऐसी प्रणाली में, एकाग्रता में परिवर्तन का एकमात्र कारण है साथएक रासायनिक प्रतिक्रिया है। इस विशेष मामले के लिए
एक रासायनिक प्रतिक्रिया की दर शामिल पदार्थों की सांद्रता और तापमान पर निर्भर करती है।
कहां क- एक रासायनिक प्रतिक्रिया की दर स्थिर, सी ए, सी बी- पदार्थों की एकाग्रता, एन 1, एन 2- संबंधित पदार्थों के लिए आदेश। इस अभिव्यक्ति को भौतिक रसायन विज्ञान में सामूहिक क्रिया के नियम के रूप में जाना जाता है।
सांद्रता मान जितना अधिक होगा, रासायनिक प्रतिक्रिया की दर उतनी ही अधिक होगी।
आदेश ( एन) प्रयोगात्मक रूप से निर्धारित किया जाता है और रासायनिक प्रतिक्रिया के तंत्र से जुड़ा होता है। आदेश एक पूर्णांक या भिन्नात्मक संख्या हो सकता है, कुछ पदार्थों के लिए शून्य-क्रम प्रतिक्रियाएं भी होती हैं। अगर आदेश है मैं-वाँ पदार्थ शून्य के बराबर है, तो रासायनिक प्रतिक्रिया की दर इस पदार्थ की सांद्रता पर निर्भर नहीं करती है।
रासायनिक प्रतिक्रिया की दर तापमान पर निर्भर करती है। अरहेनियस कानून के अनुसार, तापमान में बदलाव के साथ दर लगातार बदलती रहती है:
कहां ए- पूर्व-घातीय कारक;
इ- सक्रियण ऊर्जा;
आर- सार्वभौमिक गैस स्थिरांक, स्थिरांक;
टी- तापमान।
साथ ही प्रतिक्रिया के क्रम की भयावहता, सक्रियण ऊर्जा के मूल्य और प्रीएक्सपोनेंशियल कारक एक विशेष प्रतिक्रिया के लिए प्रयोगात्मक रूप से निर्धारित किए जाते हैं।
यदि कोई रासायनिक अभिक्रिया विषमांगी प्रक्रिया में की जाती है, तो उसकी दर प्रारंभिक पदार्थों की आपूर्ति और रासायनिक प्रतिक्रिया क्षेत्र से उत्पादों को हटाने की प्रक्रिया से भी प्रभावित होती है। इस प्रकार, एक जटिल प्रक्रिया होती है जिसमें प्रसार चरण (आपूर्ति, निकासी) और गतिज चरण होते हैं - वास्तविक रासायनिक प्रतिक्रिया। पूरी प्रक्रिया की गति, प्रयोग में देखी गई, सबसे धीमी अवस्था की गति से निर्धारित होती है।
इस प्रकार, प्रक्रिया (मिश्रण) के प्रसार चरण की दर को प्रभावित करके, हम पूरी प्रक्रिया की दर को समग्र रूप से प्रभावित करते हैं। यह प्रभाव पूर्व-घातीय कारक ए के मूल्य को प्रभावित करता है।
अधिकांश रासायनिक प्रतिक्रियाएं सरल नहीं होती हैं (अर्थात, वे एक चरण में नहीं जाती हैं और न ही अंत तक) - जटिल रासायनिक प्रतिक्रियाएं:
ए) एबी - प्रतिवर्ती;
बी) ए → बी; В → - लगातार;
सी) ए → बी; ए → सी - समानांतर।
एक जटिल रासायनिक प्रतिक्रिया के लिए गति का कोई एकसमान माप नहीं है... सरल के विपरीत, यहां हम प्रत्येक रसायन के बनने और नष्ट होने की दर के बारे में बात कर सकते हैं। इस प्रकार, यदि निकाय में रासायनिक अभिक्रियाएँ होती हैं और एनप्रत्येक के लिए पदार्थ एनपदार्थों का अपना गति मान होता है।
किसी भी पदार्थ के लिए, गठन और विनाश की दर इस पदार्थ की भागीदारी के साथ सभी चरणों की दरों का बीजगणितीय योग है।